| 特材品名 | 圖片 | 廠牌 | 自費單價 (A) | 健保支付單價 (B) | 保險對象負擔費用 (C=A-B、取整數) | 品項用途、療效比較 | 產品特性 | 適應症 | 應注意事項 | 副作用 | 療效比較 |
| 聯合優磨二代全人工髖關節(陶瓷巨頭對陶瓷襯墊) |  | 聯合UNITED | $154,396.00 | $39,396.00 | $115,000.00 | |
本產品由傳統健保給付金屬股骨頭置換物及聚合物PE內襯以第四代陶瓷股股頭置換物及陶瓷內襯替代,可保有關節原有功能外亦可增加使用壽明
|
風濕性關節炎 外傷後的關節炎, 或退化性關節炎患者 缺血性股股頭壞死
|
1.本醫療器材只限由醫師操作使用
|
組織反應, 不適 植入不當而引起之脫位,半脫位 神經性疾病 皮膚結痂或傷口延遲癒合
|
超耐磨 增加延長使用壽命
|
| 優磨二代人工髖關節(陶瓷巨頭對高耐磨聚乙烯襯墊) |  | 聯合UNITED | $107,396.00 | $39,396.00 | $68,000.00 | |
本產品由傳統健保給付金屬股骨頭置換物以第四代陶瓷股股頭置換物替代,可保有關節原有功能外亦可增加使用壽明
|
風濕性關節炎 外傷後的關節炎, 或退化性關節炎患者 股骨頸骨折
|
1.本醫療器材只限由醫師操作使用
|
組織反應, 不適 植入不當而引起之脫位,半脫位 神經性疾病 皮膚結痂或傷口延遲癒合
|
超耐磨 增加延長使用壽命
|
| 聯合陶瓷雙極式半人工髖關節組-DELTA |  | 聯合UNITED | $105,195.00 | $35,195.00 | $70,000.00 | |
本產品由傳統健保給付金屬股骨頭置換物以第四代陶瓷股股頭置換物替代,可保有關節原有功能外亦可增加使用壽明
|
風濕性關節炎 外傷後的關節炎, 或退化性關節炎患者 股骨頸骨折
|
1.本醫療器材只限由醫師操作使用
|
組織反應, 不適 植入不當而引起之脫位,半脫位 神經性疾病 皮膚結痂或傷口延遲癒合
|
超耐磨 增加延長使用壽命
|
| 優磨二代全髖臼植入物抗氧化高耐磨聚乙烯全髖臼內襯 |  | UNITED | $64,018.00 | $4,018.00 | $60,000.00 | |
E-XPE 材料係建構於高交聯度聚乙烯材料上的技術。將維他命 E 拌入原基材 之中成型,並透過伽瑪射線(gamma ray)照射的方式,提高聚乙烯材料分子 鏈間的交聯(cross-link)程度。由於維他命 E 的特性,可持續中和材料內的 自由基,避免材料氧化,且在植入體內後仍能持續消除於體內環境中產生的 自由基,達到長期抵抗氧化的功效。由於不需進行熱處理消滅自由基,E-XPE 材料相較於 XPE 可提升 20%的機械強度,且在老化測試下提升 4 倍的抗磨耗 能力(XPE 已較健保品降低 76%磨耗率),是為大幅提升醫療品質的優質選擇。
|
一、老年退化性髖關節炎、創傷性關節炎,類風濕性關節炎等。 二、股骨頭缺血性壞死。 三、股骨頭部或頸部的急性外傷骨折。(60 歲以上患者) 四、之前失敗的髖部手術。
|
需注意病人的選擇及可靠安全的手術判斷。所選擇的置換物組件需視病人之 年齡,一般狀況,可使用骨骼之骨質狀況,是否以前動過手術或將動什麼手 術等等而定,只有在病人擁有成熟之骨骼,才可進行置換手術。 手術後,醫師給病人的術後照顧及指示病人應注意事項是非常重要的。須依 個人訂定不同之持重,不能持重或部分持重之標準。 1.術後移動病人需小心。 2.注意勿過度施壓於手術的患部。 3.病人不可在無人幫助/無輔助器的情況下單獨做髖關節的大幅度活動。 4.術後治療需注意恢復髖關節附近肌肉的力量及逐漸地增加活動力。 5.術後需定期做 X 光檢查。
|
同使用傳統人工髖關節置換手術可能的副作用: 由於植入物是用人工材料製造,將其植入人體,以期恢復患者活動能力或減 少疼痛。然而由於這些植入物受到諸多生物學、力學和物理化學因素的影 響,而對這些影響又無法做體內評定,因此不能期望這些植入物能無限承受 正常健康骨骼的活動程度和負荷。 因活動不當、外傷或其他生物力學原因引起的髖關節植入物脫位或鬆動。 外周神經疾病、神經損傷、異位骨化等之形成,可能引起嚴重的併發症,這 些併發症包括,但不限於:生殖泌尿疾病、腸胃疾病、血栓等血管疾病、栓 塞等支氣管肺疾病、心肌梗塞甚至死亡。
|
由於產品設計幾何外型並無不同,故在術後功能性表現的恢復與使用原舊有 材料製作的產品雷同。而在長期使用下,使用 E-XPE 材料的元件具有強大的 抗老化效果,除具有優異的抗磨耗表現、降低骨溶蝕及元件鬆脫的風險外, 更可長時間維持功能性表現(因元件可長時間不受因磨耗影響外型完整性、 導致功能異常的風險)。
|
| 史賽克 股脛骨鎖定釘系統-股骨組 |  | STRYKER | $85,000.00 | $19,036.00 | $65,964.00 | |
本產品主要針對左、右腳之骨折設定,符合人體長骨型態,其材質本身為鈦合金強度較一般健保不銹鋼強、輕、減低感染之風險。而內固定本身之鏍孔具多角度鎖定,可以確保內固定釘在骨髓腔裡不會鬆脫、自轉,確保植入後骨折復原之完整性。
|
主要用於開放或閉合之長骨骨折、多碎片骨折、斷片骨折、近端或遠端骨折內固定術。
|
組件若使用不當不能維持充分供血和提供牢固的固定,有可能導致器械和骨骼鬆脫、彎曲、粉碎或折斷。
|
骨折部位延遲癒合或不癒合,且由於骨折部位不癒合會造成負荷增加,有可能導致植入物斷裂,若有骨質鬆動、骨軟化、糖尿病、血管再生障礙,骨質形成不足之疾病會導致植入物鬆動、變形、裂開或斷裂。早發或遲發性感染,包括深部或表層感染,深部靜脈血栓、缺血性壞死、損傷的骨折或骨折部位短縮。
|
材質本身為鈦合金強度較一般健保不銹鋼強、輕、減低感染之風險。而內固定本身之鏍孔具多角度鎖定,可以確保內固定釘在骨髓腔裡不會鬆脫、自轉,確保植入後骨折復原之完整性。
|
| 史賽克 股脛骨鎖定釘系統-脛骨組 |  | STRYKER | $85,000.00 | $19,036.00 | $65,964.00 | |
本產品主要針對左、右腳之骨折設定,符合人體長骨型態,其材質本身為鈦合金強度較一般健保不銹鋼強、輕、減低感染之風險。而內固定本身之鏍孔具多角度鎖定,可以確保內固定釘在骨髓腔裡不會鬆脫、自轉,確保植入後骨折復原之完整性。
|
主要用於開放或閉合之長骨骨折、多碎片骨折、斷片骨折、近端或遠端骨折內固定術。
|
組件若使用不當不能維持充分供血和提供牢固的固定,有可能導致器械和骨骼鬆脫、彎曲、粉碎或折斷。
|
骨折部位延遲癒合或不癒合,且由於骨折部位不癒合會造成負荷增加,有可能導致植入物斷裂,若有骨質鬆動、骨軟化、糖尿病、血管再生障礙,骨質形成不足之疾病會導致植入物鬆動、變形、裂開或斷裂。早發或遲發性感染,包括深部或表層感染,深部靜脈血栓、缺血性壞死、損傷的骨折或骨折部位短縮。
|
材質本身為鈦合金強度較一般健保不銹鋼強、輕、減低感染之風險。而內固定本身之鏍孔具多角度鎖定,可以確保內固定釘在骨髓腔裡不會鬆脫、自轉,確保植入後骨折復原之完整性。
|
| 康鉑腰椎椎間盤融合器(側開型,大) |  | COMBO | $108,373.00 | $21,675.00 | $86,698.00 | |
為椎間植入物,由聚醚醚酮(PEEK)製成,並使用符合ISO 5832-3之鈦合金(Ti6AI4V)材料為X-ray顯影之用,並取尾碼2H為噴砂處理及8H為陽極處理做區分。
|
第二腰椎至第一薦椎(L2~S1)椎間盤退變之脊椎後路手術,如椎間盤摘除減壓、神經孔擴大成型等。脊柱二次手術或脊椎不穩定施行椎間盤固定手術。腰椎間隙狹窄或假性關節病變。脊柱椎體滑脫、峽部骨折、或退化造成不穩定,經使用椎弓根釘固定後之椎間盤填充用。
|
建議以脊椎內固定器加以固定,穩定性更佳。
|
應脊膜破裂、因手術創傷造成神經受損、感染、延遲癒合或不癒合、對植入物之材質過敏、植入物之抗力作使骨密度降低。
|
與健保材質不同,可分散硬力,預防下沉,促進植骨窗骨頭生長,有效防止鬆脫。
|
| 愛派司亞洲脛骨髓內釘系統組(補差額) |  | APS | $73,500.00 | $19,036.00 | $54,464.00 | |
亞洲脛骨髓內釘系統組為包含髓內釘、鎖定螺釘及末端蓋等構件組合成之金屬植入物,本系統組適用於脛骨幹、骨幹端及脛骨上、下端之關節內的骨折固定。
|
亞洲脛骨髓內釘為適用於脛骨幹、骨幹端及脛骨上、下端之關節內的骨折固定,本系統適應之脛骨骨折分類包含:
1. 脛骨近端A2及A3型骨折(41-A2/A3)。
2. 脛骨骨幹骨折。
3. 脛骨遠端A1、A2及A3型骨折(43-A1/A2/A3)。
4. 混合上述類型骨折。
|
不當的術後活動可能造成植入物破壞,術後請依循醫囑活動。
|
1. 植入物變形或失效的起因在於規格選擇錯誤或內固定過度負荷。
2. 過敏反應起因於無法適應植入物材質。
3. 骨癒合延緩起因於血液循環障礙。
4. 植入物引起的疼痛或不適感。
|
1.亞洲脛骨髓內釘具有優於傳統健保髓內釘的斜行交鎖螺釘固定,即成角穩定交鎖系統(ASLS),可以同時增強骨折斷端軸向和橫向的穩定性。
2.治療脛骨複雜骨折具有固定牢靠,手術創傷小,手術時間短等優點,是治療脛骨複雜骨折比較理想的內固定方法。
|
| 百優螺釘固定式陶瓷人工髖關節組 |  | ZIMMER | $142,396.00 | $39,396.00 | $103,000.00 |  品項用途 品項用途 |
第四代陶瓷高耐磨度,抗碎裂大幅減少植入物間的磨損。大直脛股骨頭可增加病人的活動角度。
|
1.關節因退化、創傷後或風濕性疾病而產生磨損之關節炎。
2.股骨頭缺血性壞死。
3.近端股骨變形或是因先前的內固定裝置而無法植入股骨柄。
4.髖關節有高度脫臼風險者。
|
病人的體重勿過重【尤其是超過225磅(100kg)】
|
負重過大、身體活動量大可能會有植體鬆脫或碎裂的問題。
|
1較一般金屬頭塑膠墊片的耐磨度高,使用年限延長。
|
| CERAMIC TOTAL HIP SYSTEM陶瓷全人工髖關節 |  | OSTEONICS | $102,396.00 | $39,396.00 | $63,000.00 |  品項用途 品項用途 |
此系統包括金屬髖臼杯和可選擇的髖臼墊,髖臼杯不需用骨水泥固定,采登特髖臼墊可搭配任何適用之骨股柄使用,采登特陶製植入物需和鋁製股骨頭搭配使用,鈦合金接頭是用於有鋁製股骨頭和氧化鋯的骨柄,但不可用於鈦合金的骨柄,圓孔、骨釘、墊片為選擇性產品,可用來固定髖臼杯。
|
退化性關節炎、風濕性關節炎、創傷所致關節炎、或最後一級缺血性壞死所造成的關節疼痛或功能喪失。在臨床上之關節固定術,或替代的重建技術未達滿意,股骨近端骨折、失敗的股骨置換物。
|
需徹底了解植入物的特性及使用方法且確實遵守建議事項,特別是陶製組件之組裝將影響手術的成功與否,需依X光片選用適當的植入物。
|
由於許多生物學、力學和物理化學上的因素影響內植物,植入組件無法承受如健康般的骨頭一樣的活動負荷,脫位、鬆脫、斷裂等,手術中可能造成股骨柄、髖臼窩或大轉子裂縫、穿孔等 。
|
耐磨性增加,可減少人工髖關節置換後的磨損,增進人工髖關節的使用期限。
|
| 陶瓷雙極式半人工髖關節組(黃陶) |  | 史賽克 | $67,195.00 | $35,195.00 | $32,000.00 |  品項用途 品項用途 |
耐磨、增加使用年限。
|
1.因退化性關節炎、風濕性關節炎、創傷所致關節炎或最後一級的缺血性壞死所造成的關節疼痛或功能喪失。
2.在臨床上關節固定術,或替代的重建技術未達到滿意的結果。
3.股骨近端骨折、骨頭流失,臨床上需要切短股骨高度之狀況。
4.失敗的股骨頭置換術、髖臼窩整型之重建手術。
|
需徹底了解植入物的特性
及使用方法且確實遵守建議事項,特別是陶製組件之組裝將影響手術的成功與否,需依X光片選用適當的植入物。
|
由於許多生物學、力學和物理化學上的因素影響內植物,植入組件無法承受如健康般的骨頭一樣的活動負荷,脫位、鬆脫、斷裂等,手術中可能造成股骨柄、髖臼窩或大轉子裂縫、穿孔等 。
|
比一般健保產品耐磨,患者術後復原良好
|
| 粉紅陶瓷股骨頭TRIDENT CERAMIC FEMORAL HEAD |  | STRYKER | $54,352.00 | $4,352.00 | $50,000.00 | |
產品材質為第四代粉紅陶瓷製品,較前代黃色陶瓷更耐磨,磨擦係數更小避免活動時異音的產生,.病患活動更加平順自如.
|
股骨頸骨折,退化性關節炎,風濕性關節炎,骨腫瘤, 外傷引起之相關性病變
|
本醫療器材只限由醫師操作使用
|
若發生感染可能導致治療失敗,脫位,鬆脫,極少數引起陶瓷材質之斷裂,
|
健保給付之產品材質為鈦合金或不銹鋼成分,摩擦係數高易磨損相對陶瓷產品使用壽命短少許多50倍以上,是健保產品無可比擬.
|
| 陶瓷半人工髖關節組(粉陶)CERAMIC BIPOLAR SYSTEM |  | STRYKER | $90,195.00 | $35,195.00 | $55,000.00 | |
耐磨、增加使用年限。
|
1.因退化性關節炎、風濕性關節炎、創傷所致關節炎或最後一級的缺血性壞死所造成的關節疼痛或功能喪失。
2.在臨床上關節固定術,或替代的重建技術未達到滿意的結果。
3.股骨近端骨折、骨頭流失,臨床上需要切短股骨高度之狀況。
4.失敗的股骨頭置換術、髖臼窩整型之重建手術。
|
需徹底了解植入物的特性
及使用方法且確實遵守建議事項,特別是陶製組件之組裝將影響手術的成功與否,需依X光片選用適當的植入物。
|
由於許多生物學、力學和物理化學上的因素影響內植物,植入組件無法承受如健康般的骨頭一樣的活動負荷,脫位、鬆脫、斷裂等,手術中可能造成股骨柄、髖臼窩或大轉子裂縫、穿孔等 。
|
比一般健保產品耐磨,患者術後復原良好
|
| 史賽克伽瑪三股骨固定系統-長釘組 | 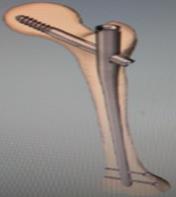 | STRYKER | $72,800.00 | $19,036.00 | $53,764.00 |  品項用途 品項用途 |
本系統是供臨時固定、矯正或穩定骨骼的醫療器械,僅供單次使用,這些植入物包括不同款式的內固定器械及配件,在處理骨折及重建手術中使用這些器械能提供骨固定之途徑。但這些器械只能補助骨骼癒合,不能替代正常的骨結構物,本產品主要用於骨折斷端或骨碎片的暫時穩定,直到骨骼癒合為止。
|
骨折固定、截骨術、關節融合、畸形矯正、重建手術或其他治療。本系統主要適用於粗隆骨下骨折,股骨轉子合併骨幹骨折,於粗隆及長骨部位之病理骨折包含預防之作用,骨折不接合和癒合不良。本系統骨釘組適用於高度骨鬆之股骨頭,短股骨頭/頸斷裂,股骨轉子不穩固或粗隆間骨折中尾部內無骨頭支撐。本系統之粗隆骨固定釘適用於粗隆間骨折,骨股轉子骨折,骨折不接合和癒合不良。
|
術前注意事項:該植入物僅供單次使用,與體液接觸過支植入物不得再次使用。
術中注意事項:避免植入物表面受損,避免將植入物塑型成彎曲,除非其他用途,否則此產品不可與其他製造廠商的產品共用。
術後注意事項:該植入物是一種短期的產品。在骨延遲癒合、不癒合或植入物未被取出等情況下可能導致併發症。
|
骨折部位延遲癒合或不癒合,由於延遲癒合造成負荷增加,植入物有可能會斷裂;不穩定得粉碎性骨折,骨折斷端周圍纖維組織反應性增生、早發或遲發性感染、深部靜脈血栓、缺血性壞死、損傷的骨折或骨折部位短縮、手術創傷可能導致神經損傷。
|
本系統是供臨時固定、矯正或穩定骨骼的醫療器械,僅供單次使用,這些植入物包括不同款式的內固定器械及配件,在處理骨折及重建手術中使用這些器械能提供骨固定之途徑。但這些器械只能補助骨骼癒合,不能替代正常的骨結構物,本產品主要用於骨折斷端或骨碎片的暫時穩定,直到骨骼癒合為止。
|
| 沃思坦骨髓內釘系統-PFNA |  | 沃思坦 | $82,000.00 | $19,036.00 | $62,964.00 | |
以亞洲人種體型做為考量,參照亞洲人之生理弧度設計,相容性高,可依據骨折選擇需求長度及寬窄的尺寸植入,採用鎖定骨釘與骨頭密合服貼度高,融合度佳,大幅提升骨頭抓附能力,乘載強度,穩定患部以達到最佳治療果
|
1.用於骨折固定。2.長骨中段不穩定之骨折。
3.扭曲狀之骨折。4.骨折未接合及接合不全。
|
1.任何手術過程中,手術後照料是影響患者手術成功的因素,包括各種病因引起的出血性疾病、長期類固醇治療、免疫抑制劑治療或高劑量的放射治療。
2.避免人工骨過度填充或加壓於治療部位。
3.自費特材骨板骨釘仍有彎曲斷裂及螺絲鬆脫之可能,而導致骨折變形及骨折不癒合,須遵照醫師指示下進行活動。
|
1.由於植入物植入不當導致鬆脫。
2.感染:術後傷口感染及深處傷口產生敗血現象。
3.血管疾病:血栓靜脈炎、肺栓塞、傷口血腫及血管壞死。
4.肢體臠縮。
|
傳統健保NAIL與骨頭密合度、服貼度不佳,承載力量較為薄弱,因此受力後可能出現彎曲或變形的現象,患者若有骨鬆的症狀較容易造成需要進行二次手術之風險提升。
|
| 聖那美邁倢髓內釘系統-轉子髓內釘組 |  | SANATMETAL | $88,000.00 | $19,036.00 | $68,964.00 | |
髓內釘的尺寸及形狀經過設計,旨在填滿骨髓腔。大部分髓內釘均為中空設計,因此可使用套管術。髓內釘用於恢復骨骼在骨折前的形狀。髓內釘有多種長度及直徑,適用於不同的解剖構造。
|
用於穩定骨骼及修復骨折。
|
應遵照醫師指示使用。
|
對金屬材質過敏。
|
1.鈦合金材質,生物相容性高。2.鎖定骨釘提供角穩定度,使植入物更加堅固穩定。3.髓內釘依據人體解剖設計,能更符合人體結構,使其穩定性高。4.動力加壓系統,使骨頭癒合復原。5.遠端鎖定系統,減少手術時間。
|
| 聖那美邁倢髓內釘系統-股骨髓內釘組 |  | SANATMETAL | $85,000.00 | $19,036.00 | $65,964.00 | |
髓內釘的尺寸及形狀經過設計,旨在填滿骨髓腔。大部分髓內釘均為中空設計,因此可使用套管術。髓內釘用於恢復骨骼在骨折前的形狀。髓內釘有多種長度及直徑,適用於不同的解剖構造。
|
用於穩定骨骼及修復骨折。
|
應遵照醫師指示使用。
|
對金屬材質過敏。
|
1.鈦合金材質,生物相容性高。2.鎖定骨釘提供角穩定度,使植入物更加堅固穩定。3.髓內釘依據人體解剖設計,能更符合人體結構,使其穩定性高。4.動力加壓系統,使骨頭癒合復原。5.遠端鎖定系統,減少手術時間。
|
| 聖那美邁倢髓內釘系統-脛骨髓內釘組 |  | SANATMETAL | $85,000.00 | $19,036.00 | $65,964.00 | |
髓內釘的尺寸及形狀經過設計,旨在填滿骨髓腔。大部分髓內釘均為中空設計,因此可使用套管術。髓內釘用於恢復骨骼在骨折前的形狀。髓內釘有多種長度及直徑,適用於不同的解剖構造。
|
用於穩定骨骼及修復骨折。
|
應遵照醫師指示使用。
|
對金屬材質過敏。
|
1.鈦合金材質,生物相容性高。2.鎖定骨釘提供角穩定度,使植入物更加堅固穩定。3.髓內釘依據人體解剖設計,能更符合人體結構,使其穩定性高。4.動力加壓系統,使骨頭癒合復原。5.遠端鎖定系統,減少手術時間。
|
| 瑞寶億里貝斯彈性椎間融合器(大CAGE) |  | ReBorn | $77,002.00 | $15,400.00 | $61,602.00 |  品項用途 品項用途 |
1.榮獲國家品質標章
2.台灣市場為一具有彈性功能的腰椎
椎間融合器,符合人體腰椎生理動態.
3.表面多孔隙設計符合人體骨小樑孔隙
達到骨誘導目的完成錐體骨結合效果
有效防止融合器鬆脫情況發生.
4.融合器中間具植骨窗設計更能再次加
強植體穩定效果
5.產品設計依人體腰椎間終端骨板幾何
結構設計,每節只需植入一顆.手術簡
單 ,減少術中出血量,病患復原速度快.
6.規格齊全,完全符合國人腰椎尺寸需求
|
頸椎椎間盤蛻變之脊椎前路手術(由脊椎前方植入之手術方法)。頸椎脊柱脫位、滑脫與不穩定之治療與二次手術之重建。
|
須經專科醫師使用
嚴重的骨質疏鬆症及創傷
或病症之椎體有活動期之感染不宜施行
|
無
|
健保給付目前為固定式金屬棒狀,不具可彎曲性.
|
| 康鉑頸椎椎間盤融合器 |  | COMBO | $66,090.00 | $13,218.00 | $52,872.00 |  品項用途 品項用途 |
康鉑頸椎椎間融合器為脊椎手術的植入裝置,用於作為頸椎椎間的填充塊,有支撐與穩定椎脊之功效,康鉑頸椎椎間融合器為圓方體中央有上下方向的孔洞,可填入骨頭或骨替代物,促進脊椎融合。植入物有不同的尺寸大小,可依 具患者的需求而選用。融合器材質為符合ASTM F2026之聚醚醚酮(peek)製成,並使用符合ASTM F136 之鈦合金材料為X-Ray顯影之用,並取尾碼2H為噴砂處理及8H為陽極處理做區分。
|
頸椎椎間盤蛻變之脊椎前路手術(由脊椎前方植入之手術方法)。頸椎脊柱脫位、滑脫與不穩定之治療與二次手術之重建。
|
本產品建議須與頸椎固定器一併使用,穩定性更佳。在每一椎傑內僅可放置一顆"椎間融合器",器械使用前須經高溫高壓消毒滅菌後方可使用。
|
可能造成硬脊膜破裂、手術創傷造成神經受損、感染、對植入物材質過敏、延遲癒合或不癒合、植入物之抗力作使骨密度降低。
|
健保給付目前為固定式金屬棒狀。
|
| 康鉑腰椎椎間盤融合器(小) |  | COMBO | $67,305.00 | $13,461.00 | $53,844.00 | |
康鉑腰椎椎間盤融合器為椎體間植入物,由聚醚醚酮(peek)製成,並使用符合ISO 5832-3 之鈦合金材料為X-Ray顯影之用,並取尾碼2H為噴砂處理及8H為陽極處理做區分。
|
第二腰椎至第一薦椎椎間盤蛻變之脊椎後路手術,如椎間盤摘除減壓、神經恐擴大成型等,脊柱二次手術或脊柱不穩定施行椎間盤固定手術,腰椎間係狹窄或假性關節病變,脊椎椎體滑脫、峽部骨折、或退化造成不穩定,經此用椎弓根釘固定後之椎間盤填充用。
|
建議以脊椎內固定器加以固定,穩定性更佳,可在兩個融合器之間隙植骨,做堆體融合術或後側方植骨融合術,除非病患生理解剖或手術部位暴露不族等因素外,應盡可能每一椎節放置兩個"椎間盤融合器"。
|
可能造成硬脊膜破裂、手術創傷造成神經受損、感染、對植入物材質過敏、延遲癒合或不癒合、植入物之抗力作使骨密度降低。
|
健保給付目前為固定式金屬棒狀。
|
| 陶瓷全人工髖關節組(粉陶)CERAMIC TOTAL HIP SYSTEM |  | STRYKER | $89,396.00 | $39,396.00 | $50,000.00 | |
此系統包括金屬髖臼杯和可選擇的髖臼墊,髖臼杯不需用骨水泥固定,采登特髖臼墊可搭配任何適用之骨股柄使用,采登特陶製植入物需和鋁製股骨頭搭配使用,鈦合金接頭是用於有鋁製股骨頭和氧化鋯的骨柄,但不可用於鈦合金的骨柄,圓孔、骨釘、墊片為選擇性產品,可用來固定髖臼杯。
|
退化性關節炎、風濕性關節炎、創傷所致關節炎、或最後一級缺血性壞死所造成的關節疼痛或功能喪失。在臨床上之關節固定術,或替代的重建技術未達滿意,股骨近端骨折、失敗的股骨置換物。
|
需徹底了解植入物的特性及使用方法且確實遵守建議事項,特別是陶製組件之組裝將影響手術的成功與否,需依X光片選用適當的植入物。
|
由於許多生物學、力學和物理化學上的因素影響內植物,植入組件無法承受如健康般的骨頭一樣的活動負荷,脫位、鬆脫、斷裂等,手術中可能造成股骨柄、髖臼窩或大轉子裂縫、穿孔等 。
|
耐磨性增加,可減少人工髖關節置換後的磨損,增進人工髖關節的使用期限。
|
| 史賽克肱骨/近端肱骨鎖定系統特材(組) |  | STRYKER | $85,000.00 | $19,036.00 | $65,964.00 | |
本系統是供臨時固定、矯正或穩定骨骼的醫療器械,可用於癒合不良和骨不接合時使用,僅供單次使用。
|
主要提供肱骨各種不同型態的骨折及肱骨近端或骨幹骨折。
|
避免植入物表面受損,手術過程中需反覆檢查植入物與器械間連接牢靠,以確保定位精確,此植入物是一種短期產品。
|
骨折部位延遲癒合或不癒合,若造成負荷增加,植入物可能斷裂,骨不癒合,骨質鬆動、骨軟化、糖尿病、血管再生障礙等可能導致植入物鬆動、變形、裂開。
|
無
|
| 英特格堤飛爾霍克腰椎椎間融合系統 |  | INTEGRITY | $159,707.00 | $31,941.00 | $127,766.00 | |
與硬質骨彈性係數相近的PEEK外殼結合Titanium墊片,可經由工具進行高密度植骨以提升融合率,目前唯一可擴展式椎間盤融合器中,高度與寬度能夠達到同時展開,提供椎間盤內更多的乘載面積,進而降低融合器可能造成之風險如沉降
|
本產品可搭配由疏鬆骨或(和)皮質疏鬆骨組成之自體和(或)異體移植骨運用於椎間融合術,適用於L2至S1間一或二個連續節段的退化性椎間盤疾病的病患。
|
應依據醫囑術後休憩臥床,避免其他過度運動以減少植體承受過度負載的風險,否則可能會損害植體完整性或延遲癒合過程。若要活動宜穿戴輔具,且不宜過度彎曲伸展,或是提取重物抑或是做劇烈運動,以免造成植入產品在未達融合效果前位移。
|
植入物輕微移位 (Migration)、沉陷、斷裂、失去固定、椎骨骨折、神經系統或血管或內臟受損,某些退化性疾病或潛在的生理疾病如糖尿病,類風濕關節炎或骨質疏鬆症可能會改變癒合過程,從而增加植入物斷裂或脊柱骨折的風險。與那些以前沒有手術的人相比,曾接受此脊柱外科手術的患者可能會有不同的臨床結果。
|
目前尚無健保類似品(可撐開式融合器)可比較
|
| 帶線迷你固定錨釘2.0MM PEEK WITH 1 ULTRABRAID |  | SMITH | $24,715.00 | $9,886.00 | $14,829.00 | |
用於連接肩、足、踝、肘、膝各病症之軟組織與骨頭
|
1.2.0mm微創手術專用,PEEK材質。
2.提供2-0 Ultrabraid縫線,強度佳。
3.用於連接肩、足、踝、肘、膝各病症之軟組織與骨頭
|
1. 本產品係以無菌提供,只能單次使用,不要重新滅菌,過期時請不要使用,請丟
棄開封未使用之產品
2.使用前醫師應熟悉適當的手術技巧
3.使用前請詳閱使用說明
4.錨釘沒有完全插進會造成錨釘的固定功能不佳
5.植入前,若植入點沒有事先準備好,可能會導致錨釘斷掉
6.不要嘗試將錨釘植入在生長軟骨板內或非骨質的組織
7.在確認錨釘適當放入插入器前,切勿移開縫線滯留器,否則可能會導致錨釘脫
落而掉入關節內
8.轉動鈕左旋即可以鬆開錨釘栓,而過度的旋轉會將內錨釘移位,可能導致錨釘
栓損壞或從插入器脫落,而掉入關節內,旋開轉鈕時,足夠允許縫線容易活動即
可
|
1、輕微發炎反應的可能性發生。
2、過敏反應的可能性。
3、深層及淺層感染的可能性。
|
1.2.0mm微創手術專用,PEEK材質。
2.提供2-0 Ultrabraid縫線,強度佳。
|
| 5.5MM雙圈免綁線螺旋固定錨釘(阿碩柯爾 縫合錨釘) |  | 阿碩柯爾 | $24,715.00 | $9,886.00 | $14,829.00 | |
1.雙Loop設計,可達四條帶線功能,植入操作快速又穩固2.主體正反轉旋入,錨釘內部雙層固定構造設計
|
適用於連接軟組織於肩、足、踝、肘、膝、手、腕與髖骨頭上之固定
|
單一次性使用
|
無
|
健保品項帶線錨釘為金屬材質,患者痊癒之後,金屬錨釘會留在骨頭裡,少數患者會感到異物感
|
| TM-S CAGE CERVICAL 多孔鉭金屬椎體替代系統(頸椎) |  | ZIMMER | $47,456.00 | $9,491.00 | $37,965.00 | |
1.高開孔率結構,與人體海綿骨極度接近,可使骨頭生長至融合器內部深源,提供更大範圍的融合面積。可達成早期骨融合效果,讓病人在更短時間內回復。。2.材質軟硬度比聚醚醚酮(PEEK) 椎間融合器更接近人體海綿骨,減少融合器術後的下沉 (subsidence) 問題。
3.材質擁有高摩擦係數可增加融合器的穩定度,減少術後 cage migration 問題。增加植入物安全性。
|
多孔鉭金屬椎體替代系統適用於頸椎C3到胸椎T1有症狀性椎間盤疾病病人的融合手術.
|
本產品需按醫師指示使用。
|
無
|
1.骨頭可長進融合器內 ,提供更大範圍的融合面積。可達成早期骨融合效果,讓病人在更短時間內回復。2.軟硬度接近人體骨頭. 3.高摩擦係數表面可增加融合器的穩定度。
|
| 艾易特頸椎融合器(前) CE14040S:CE14090S |  | 艾易特 | $95,825.00 | $19,165.00 | $76,660.00 | |
1.本產品為使用雷射粉末燒結(Selective Laser Melting)製成的鈦合金植入物。
2.適用於前路頸部椎間盤切除融合手術(ACDF)提供頸椎前路的穩定性。
|
1. 本產品為椎間體融合器,適用於經成像報告(放射線、CT、MRI)證實有椎間退化或頸椎不穩定所導致頸椎(C2-T2)症狀。
2. 頸椎多個椎體神經根、脊髓病變或疼痛的骨骼發育成熟病患之頸椎前路椎體融合。
3. 退化性椎間盤疾病(椎因性疼痛、脊椎狹窄等)皆適用。
|
1. 需具備全面指示操作和確立概念性方面的操作技術 。
2. 主要頸椎嚴重滑脫,需評估是否適用。
3.建議在X光影像下施作以確保位置正確。
|
1. 外力撞擊下使植入物鬆脫位移。
2. 對植入物有過敏反應。
3. 植入物不適感引起的疼痛。
4. 融合脊椎層相鄰脊椎的退化性變化或不穩固。
5. 伴有癱瘓或失去知覺的脊椎壓縮。
|
此自費品項因為器械設計以及植入物製成不同,可使病人手術後回復期縮短,並大幅提高骨融合的成功機率。
|
| PM2152聖猷達恩德拉第心臟節律器-雙腔(DDDR+MRI) |  | SJM | $109,833.00 | $93,833.00 | $16,000.00 | |
Endurity Core PM2152 雙腔節律器,可作條件式核磁造影,本產品可配合Merlin程式調節系統來進行程式調節,且具備運動功能可依據病人活動狀態調節心律。
|
本產品適用於以下適應症,包含暈厥、暈厥前兆、疲勞、心律不整導致的頭暈,以及綜合以上症狀。適用的病人狀況包含病竇症候群、慢性而有症狀的第二、第三房室阻滯等。
|
對於慢性心房撲動、慢性心房顫動、或心防靜止的病人,雖然不禁止使用,但其雙腔節律的效果可能不會優於單腔節律。
|
植入任何節律系統的相關潛在併發症如下:
額外的手術、過敏反應、心律失常、血管損傷(例如燙傷)、失償心臟衰竭、死亡、栓塞、侵蝕(Erision)、心臟外刺激、血腫、感染、失去心臟節律、失去同步性(Loss of synchrony)、氣胸
|
與目前現有的健保品項相比,多了
1.運動功能,可以依據病人活動適時調節心律
2.可做到1.5T MRI
3.有遠端照護系統,未來可配合醫院及病患需求,給予更完善及時的照護
|
| X2DR01 美敦力 亞士卓磁振造影植入式心臟節律器 |  | MEDTRONIC | $153,833.00 | $93,833.00 | $60,000.00 | |
本產品為雙腔植入式心臟節律器,是一種能設定多項程式的心臟用裝置,可監測並調控病患的心跳速率,提供單腔或雙腔的速率反應緩脈節律治療與心房頻脈心律不整治療。
|
本產品適用可受益於速率反應或非速率反應節律的病患使用,以恢復生理性心跳速率、改善心輸出量、預防症狀、或避免與心臟脈衝形成或傳導障礙有關的心律不整。
|
1. 在進行MRI掃描前,請先參閱Medtronic MRI技術手冊,了解MRI相關的警語及注意事項。
2. 關於醫療和診斷程序對植入心臟裝置病患危害的相關資訊,請參閱原廠說明書「Medical Procedure and EMI Warnings and Precautions Manual」,內容也包括病患環境中的電磁干擾源(EMI)的資訊。
3. 抗凝血治療-使用本產品時,不應改變既有抗凝血治療的使用。
4. 植入期間保持電絕緣-植入時,切勿讓病患接觸到可能會漏電的接地設備。漏電可能會引起頻脈心律不整,進而導致病患死亡。
5. 體外去顫設備-在本產品測試、植入過程或植入後的測試期間,為了因應任何有可能或蓄意引發的頻脈心律不整,均需將體外去顫設備置於附近,以供隨時取用。
6. 導線相容性-請勿使用未經原廠驗證與Medtronic裝置相容之其它廠牌導線。若導線無法與Medtronic裝置相容,結果可能會導致心臟活動的感測不足(undersensing)、無法傳輸必要的治療,或產生漏電或間歇性電流。
7. 一個完整的SureScan節律系統包括一個接有SureScan導線的SureScan裝置。進行MRI掃瞄前,請參閱原廠說明書「MRI Technical Manual」。
|
使用導線與節律系統時可能引發的不良事件,包括但不限於空氣栓塞、不當加速的心律不整、過敏反應、感染、出血、疤腫形成、身體排斥現象(包括局部組織排斥)、導線磨損及斷裂、心臟剝離、導線移動/脫離、心臟穿孔、 肌肉及神經刺激、心包填塞、心肌損害、慢性神經損傷、心肌過度敏感、死亡、肌電位感測、栓塞、心包膜積水、心內膜炎、心包摩擦音、裝置與導線侵蝕穿透皮膚、氣胸、過度纖維化、閾值升高、擠壓、血栓性栓塞、纖維顫動或其它心律不整、血栓、體液聚積、經靜脈導線相關之血栓、形成囊腫、瓣膜損害(特別是虛弱的心臟)、心電傳導阻斷、靜脈閉塞、心臟壁破裂、靜脈穿孔、血腫/血清腫、靜脈壁破裂。
|
參考品項:美敦力黛拉心臟節律器
與全額給付品項不同的附加功能為:
1. 具速率反應模式,可適用於運動耐受力不足或因心律不整而有運動限制的病患,例如病竇症候群。
2. 具心房頻脈治療功能,可自動偵測心房頻脈並給予心房抗頻脈快速刺激(Atrial ATP),研究顯示開啟此功能可減少62%永久性心房顫動的發生率 ,並相對減少與心房顫動相關的住院率(42%)及急診報到率(68%) 。
3. 具體液狀態監測,可藉由經胸腔電阻值的變化可協助推估病患胸腔體液累積的程度,研究證實與體重監測(敏感度22.5%)相比,經胸腔電阻值監測(敏感度76.4%)能更準確預測心衰竭惡化 。
|
| 安速拉第核磁共振心臟節律器 Assurity MRI PM2272 |  | ABBOTT | $153,833.00 | $93,833.00 | $60,000.00 | |
1.可以在核磁共振的環境中有條件的(1.5T)安全使用的節律器; 2.可接受全身核磁共振掃描(無檢查部位之限制); 3.可承受較高的檢查能量(4W/Kg); 4.具AF完整管理系統;5.自動心律調整功能; 6.具無線程控及無線資料傳輸功能。
|
病竇症候群 有症狀的第二級房室傳導阻斷 第三級(完全)房室傳導阻斷 有症狀的心房顫動合併心室速率過慢 心臟手術後不可逆的心臟傳導阻斷 經導管電燒治療所導致的嚴重心臟傳導阻斷 迷走神經反應異常導致心跳過緩引起昏厥
|
1.保持傷口的清潔與乾燥以預防感染; 2.手術側上肢四到六週內應避免大幅度之活動以免導線脫落或移位。
|
可能之併發症有注射處血腫、動脈穿刺、危險性心律不整、氣胸、血胸、肺栓塞、導線位置不良、心臟破裂、局部或全身感染。
|
健保給付之傳統心臟節律器無法接受核磁共振檢查。
|
| W3DR01亞士爾磁振造影植入式心臟節律器-雙腔 |  | MEDTRONIC | $128,833.00 | $93,833.00 | $35,000.00 |  品項用途 品項用途 |
本產品為雙腔植入式心臟節律器,是一種能設定多項程式的心臟用裝置,可監測並調控病人的心跳速率,提供單腔或雙腔的速率反應緩脈節律治療與心房頻脈心律不整治療。是透過偵測心臟活動的感測器來進行控制。MRI SureScan 功能提供一種操作模式,此模式允許植入 SureScan 系統的病患可在裝置持續提供適當的緩脈節律治療 的同時,能安全地進行 MRI 掃描。
|
適用於長期需要心臟節律治療的病患,無行動能力、迷走神經性昏厥、心房頻脈等病患,且有進行磁振造影檢查的需求。
|
回診追蹤檢查:需定期返院檢查及定時規則服藥,若感暈厥、心悸、胸痛、倦怠、下肢腫脹、連續或數頻打嗝,應返診。
|
潛在的不良反應(任何植入心臟節律器相關的併發症):
1.血栓、氣栓的形成、栓塞。
2.氣胸、血胸、血腫。
3.傷口感染,局部組織排斥或纖維化。
4.導線位移或穿孔導致心包填塞。
|
1. 此新型之節律器具備能依病患之運動及生理需求做心跳速率之調節
2. 可和核磁共振影像檢查相容。 3.具有藍芽無線功能技術,實現安全的無線支援進行遠端監控 ,且不會影響電池使用壽命。
|
| 艾尼傳磁振造影植入式心律調節器-(雙腔)DR-T 407147 | 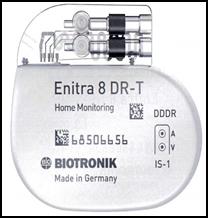 | BIOTRONIK | $145,833.00 | $93,833.00 | $52,000.00 | |
本產品系列裝置具有特殊版本的速率調適功能:利用生理阻抗測量功能發現心輸出量需求升高。測量原理是以心肌收縮性的變化(離子移變作用)為基礎(CLS功能:封閉迴路刺激[Closed Loop Stimulation])。在封閉迴路刺激模式中,速率調適功能會自動啟動及調整。本產品Enitra 8在感測器的協助下,能可靠地辨識磁振造影裝置的靜磁場。這項感測器可在讀取時利用MRI AutoDetect 功能啟動,時間最長14天。如果患者在設定時間內接近磁振造影裝置,植入裝置可辨識靜磁場,並自動啟動預設的磁振造影程式;待患者離開造影裝置後,會自動重新設定為永久性程式。透過Home Monitoring,診斷及治療資訊與技術資料可經由裝置頂蓋的天線自動傳送至固定式或移動式發射器。這些資料經過加密後,從發射器經行動電話網路傳送至BIOTRONIK服務中心。
|
Enitra為一系列的植入式心律調節器產品,適用於各種緩脈心律不整適應症。治療主要目的包括改善可能有臨床表現的患者症狀。植入心律調節器是一種症狀治療,目的為以心房、心室或房室循序節律的方式對緩脈進行補償。
|
1.傷口照護及活動方面:裝置後1個月內確保傷口乾淨乾燥,若傷口有感染徵象:如紅腫熱痛及分泌物,須立即回診。
1個月內勿將手臂高舉過頭,1-3個月內應避免影響患肩急速或劇烈的活動如游泳、打籃球、提重物等。
2.電氣設備:一般環境中電器設備都不會危害您的節律器,但須避免出入高電量(如大型發電機或馬達)及高壓電線。
其他醫療檢查及手術治療前(如:核磁共振掃瞄(MRI)、體外去顫術、體外碎石術..等)須先告知醫師裝有心臟節律器,
以防止儀器受干擾或破壞。
3.裝置核磁共振兼容雙腔感應型心臟節律器, 是可接受有條件核磁共振掃描檢查,請檢查3-7天前一定要先會診心臟科醫師。
|
正常併發症可能包括裝置容器內的液體累積、感染或組織反應。無法排除裝置系統的技術故障,包含導線移位、導線斷裂、絕緣缺陷或電池電力耗盡等。
|
本產品DDDR-MRI是MRI AutoDetect核磁共振兼容雙腔心臟節律器,可依生理活動自動加速或減緩心跳反應器,較符
合正常生理反應。且具備能夠可靠辨識核磁共振造影裝置的感測器。這項感測器可在讀取時利用MRI AutoDetect功能啟動,時間最長14天。本產品另有Home Monitoring居家監測系統,搭配相容的軟硬體,可提供完整的治療管理系統。一般健保品項DDD為基礎雙腔心臟節律器沒有生理活動自動加速反應器及不可接受核磁共振掃描檢查。
|
| 信迪思歐瑞克椎間植入物(前開、側開型) | 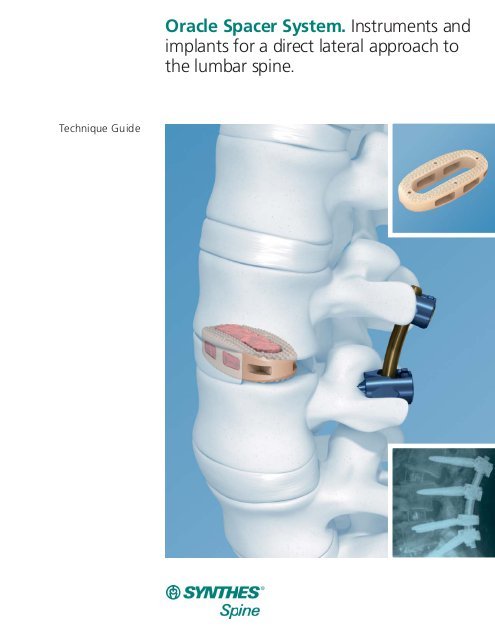 | SYNTHES | $112,936.00 | $22,587.00 | $90,349.00 | |
1. 因操作器械配備有側邊可透視撐開器,適用於OLIF及XLIF等方式放入植入物。
2. 本產品為聚合物材質,較金屬材質植入物具有彈性,不易陷入椎體內,並具有接觸面積大以及大容量植骨體積等特性,以增加椎間融合穩定度。
|
1.用於取代L1-L5腰椎椎間盤並且以融合方式將鄰近椎體融合。腰椎間盤退變疾病和脊柱不穩定。
2. 椎間切除術後所產生併發症的重建手術。
3. 先前已做過椎間盤置換術但仍有症狀需在次手術的患者。
4. 假關節或失敗的關節手術。
5. 退化性脊椎滑脫症。
6. 峽部脊椎滑脫症。
|
1. 骨鬆程度過高需評估是否需搭配骨釘固定。
2. 主要脊柱不穩定,需評估是否適用。
3.建議在X光影像下施作以確保位置正確。
|
1. 外力撞擊下使植入物彎曲斷裂或鬆脫位移。
2. 對植入物有過敏反應。
3. 植入物不適感引起的疼痛。
4.因特殊體質的血液循環系統障礙而造成的癒合遲緩。
|
此自費品項因為器械設計不同以及手術術式的不同,使患者手術傷口減小減少週邊肌肉破壞,可使病人手術後回復期縮短,並大幅提高骨融合的成功機率。
|
| 2.25 x 8 mm冠狀動脈塗藥支架系統H7493941708220 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.25 x 8 mm冠狀動脈塗藥支架系統H7493941708220 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.25 x 12 mm冠狀動脈塗藥支架系統H7493941712220 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.25 x 12 mm冠狀動脈塗藥支架系統H7493941712220 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.25 x 16 mm冠狀動脈塗藥支架系統H7493941716220 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.25 x 16 mm冠狀動脈塗藥支架系統H7493941716220 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.25 x 20 mm冠狀動脈塗藥支架系統H7493941720220 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.25 x 20 mm冠狀動脈塗藥支架系統H7493941720220 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.25 x 24 mm冠狀動脈塗藥支架系統H7493941724220 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.25 x 24 mm冠狀動脈塗藥支架系統H7493941724220 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.25 x 28 mm冠狀動脈塗藥支架系統H7493941728220 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.25 x 28 mm冠狀動脈塗藥支架系統H7493941728220 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.25 x 32mm冠狀動脈塗藥支架系統H7493941732220 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.25 x 32mm冠狀動脈塗藥支架系統H7493941732220 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.25 x 38mm冠狀動脈塗藥支架系統H7493941738220 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.25 x 38mm冠狀動脈塗藥支架系統H7493941738220 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.50 x 8 mm冠狀動脈塗藥支架系統H7493941708250 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.50 x 8 mm冠狀動脈塗藥支架系統H7493941708250 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.50 x 12 mm冠狀動脈塗藥支架系統H7493941712250 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.50 x 12 mm冠狀動脈塗藥支架系統H7493941712250 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.50 x 16 mm冠狀動脈塗藥支架系統H7493941716250 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.50 x 16 mm冠狀動脈塗藥支架系統H7493941716250 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.50 x 20 mm冠狀動脈塗藥支架系統H7493941720250 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.50 x 20 mm冠狀動脈塗藥支架系統H7493941720250 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.50 x 24 mm冠狀動脈塗藥支架系統H7493941724250 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.50 x 24 mm冠狀動脈塗藥支架系統H7493941724250 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.50 x 28 mm冠狀動脈塗藥支架系統H7493941728250 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.50 x 28 mm冠狀動脈塗藥支架系統H7493941728250 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.50 x 32mm冠狀動脈塗藥支架系統H7493941732250 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.50 x 32mm冠狀動脈塗藥支架系統H7493941732250 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.50 x 38mm冠狀動脈塗藥支架系統H7493941738250 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.50 x 38mm冠狀動脈塗藥支架系統H7493941738250 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.50 x 48mm冠狀動脈塗藥支架系統H7493941748250 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.50 x 48mm冠狀動脈塗藥支架系統H7493941748250 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.75 x 8 mm冠狀動脈塗藥支架系統H7493941708270 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.75 x 8 mm冠狀動脈塗藥支架系統H7493941708270 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.75 x 12 mm冠狀動脈塗藥支架系統H7493941712270 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.75 x 12 mm冠狀動脈塗藥支架系統H7493941712270 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.75 x 16 mm冠狀動脈塗藥支架系統H7493941716270 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.75 x 16 mm冠狀動脈塗藥支架系統H7493941716270 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.75 x 20 mm冠狀動脈塗藥支架系統H7493941720270 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.75 x 20 mm冠狀動脈塗藥支架系統H7493941720270 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.75 x 24 mm冠狀動脈塗藥支架系統H7493941724270 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.75 x 24 mm冠狀動脈塗藥支架系統H7493941724270 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.75 x 28 mm冠狀動脈塗藥支架系統H7493941728270 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.75 x 28 mm冠狀動脈塗藥支架系統H7493941728270 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.75 x 32mm冠狀動脈塗藥支架系統H7493941732270 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.75 x 32mm冠狀動脈塗藥支架系統H7493941732270 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.75 x 38mm冠狀動脈塗藥支架系統H7493941738270 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.75 x 38mm冠狀動脈塗藥支架系統H7493941738270 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.75 x 48mm冠狀動脈塗藥支架系統H7493941748270 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 2.75 x 48mm冠狀動脈塗藥支架系統H7493941748270 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 3.00 x 8 mm冠狀動脈塗藥支架系統H7493941708300 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 3.00 x 8 mm冠狀動脈塗藥支架系統H7493941708300 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 3.00 x 12 mm冠狀動脈塗藥支架系統H7493941712300 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 3.00 x 12 mm冠狀動脈塗藥支架系統H7493941712300 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 3.00 x 16 mm冠狀動脈塗藥支架系統H7493941716300 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8mm,12mm,16mm,20 mm,24mm,28mm,32mm和38mm參照血管直徑大小介於2.25-4.0mm。
|
‧僅能由受過適當訓練的醫師,執行支架置入。‧僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。‧尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。‧後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。‧對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。‧請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。‧支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積(pericardial effusion)、股動脈假性血瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 3.00 x 16 mm冠狀動脈塗藥支架系統H7493941716300 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8mm,12mm,16mm,20 mm,24mm,28mm,32mm和38mm參照血管直徑大小介於2.25-4.0mm。
|
‧僅能由受過適當訓練的醫師,執行支架置入。‧僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。‧尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。‧後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。‧對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。‧請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。‧支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積(pericardial effusion)、股動脈假性血瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 3.00 x 20 mm冠狀動脈塗藥支架系統H7493941720300 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 3.00 x 20 mm冠狀動脈塗藥支架系統H7493941720300 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 3.00 x 24 mm冠狀動脈塗藥支架系統H7493941724300 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 3.00 x 24 mm冠狀動脈塗藥支架系統H7493941724300 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 3.00 x 28 mm冠狀動脈塗藥支架系統H7493941728300 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 3.00 x 28 mm冠狀動脈塗藥支架系統H7493941728300 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 3.00 x 32mm冠狀動脈塗藥支架系統H7493941732300 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 3.00 x 32mm冠狀動脈塗藥支架系統H7493941732300 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 3.00 x 38mm冠狀動脈塗藥支架系統H7493941738300 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 3.00 x 38mm冠狀動脈塗藥支架系統H7493941738300 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 3.00 x 48mm冠狀動脈塗藥支架系統H7493941748300 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 3.00 x 48mm冠狀動脈塗藥支架系統H7493941748300 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 3.50 x 8 mm冠狀動脈塗藥支架系統H7493941708350 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 3.50 x 8 mm冠狀動脈塗藥支架系統H7493941708350 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 3.50 x 12 mm冠狀動脈塗藥支架系統H7493941712350 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 3.50 x 12 mm冠狀動脈塗藥支架系統H7493941712350 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 3.50 x 16 mm冠狀動脈塗藥支架系統H7493941716350 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 3.50 x 16 mm冠狀動脈塗藥支架系統H7493941716350 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 3.50 x 20 mm冠狀動脈塗藥支架系統H7493941720350 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 3.50 x 20 mm冠狀動脈塗藥支架系統H7493941720350 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 3.50 x 24 mm冠狀動脈塗藥支架系統 H7493941724350 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 3.50 x 24 mm冠狀動脈塗藥支架系統 H7493941724350 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 3.50 x 28 mm冠狀動脈塗藥支架系統H7493941728350 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 3.50 x 28 mm冠狀動脈塗藥支架系統H7493941728350 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 3.50 x 32mm冠狀動脈塗藥支架系統H7493941732350 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 3.50 x 32mm冠狀動脈塗藥支架系統H7493941732350 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 3.50 x 38mm冠狀動脈塗藥支架系統H7493941738350 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 3.50 x 38mm冠狀動脈塗藥支架系統H7493941738350 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 3.50 x 48mm冠狀動脈塗藥支架系統H7493941748350 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 3.50 x 48mm冠狀動脈塗藥支架系統H7493941748350 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 4.00 x 8 mm冠狀動脈塗藥支架系統H7493941708400 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 4.00 x 8 mm冠狀動脈塗藥支架系統H7493941708400 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 4.00 x 12 mm冠狀動脈塗藥支架系統H7493941712400 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 4.00 x 12 mm冠狀動脈塗藥支架系統H7493941712400 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 4.00 x 16 mm冠狀動脈塗藥支架系統H7493941716400 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 4.00 x 16 mm冠狀動脈塗藥支架系統H7493941716400 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 4.00 x 20 mm冠狀動脈塗藥支架系統H7493941720400 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 4.00 x 20 mm冠狀動脈塗藥支架系統H7493941720400 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 4.00 x 24 mm冠狀動脈塗藥支架系統H7493941724400 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 4.00 x 24 mm冠狀動脈塗藥支架系統H7493941724400 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 4.00 x 28 mm冠狀動脈塗藥支架系統H7493941728400 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 4.00 x 28 mm冠狀動脈塗藥支架系統H7493941728400 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 4.00 x 32mm冠狀動脈塗藥支架系統H7493941732400 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 4.00 x 32mm冠狀動脈塗藥支架系統H7493941732400 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 4.00 x 38mm冠狀動脈塗藥支架系統H7493941738400 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 4.00 x 38mm冠狀動脈塗藥支架系統H7493941738400 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 4.5x12-32mm冠狀動脈塗藥支架系統H7493941712450 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 4.5x12-32mm冠狀動脈塗藥支架系統H7493941712450 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 5.0x12-32mm冠狀動脈塗藥支架系統H7493941716450 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 5.0x12-32mm冠狀動脈塗藥支架系統H7493941716450 |  | BOSTON | $70,899.00 | $14,099.00 | $56,800.00 | |
新能吉艾諾莉茉斯冠狀動脈塗藥支架系統(新能吉支架系統)是為一醫療器材與藥物的複合產品,包括兩種管制的要素:一醫療器材(冠狀動脈支架系統)及一組藥物產品(艾諾莉茉斯包覆在生物可分解性聚合物塗層內)。新能吉具有低初期聚合物裝載、環狀外層塗層及生物可吸收性聚合物的獨家設計,可降低血栓形成的風險以及長期要雙重抗血小板藥物治療的需要。
|
新能吉支架系統適用於改善因原發性(de novo)冠狀動脈病灶所引發有症狀之缺血性心臟病患者之冠狀動脈管腔內徑。治療的病灶長度應該小於標稱之支架長度(8 mm, 12 mm, 16 mm, 20 mm, 24 mm, 28 mm, 32 mm和38 mm)參照血管直徑大小介於2.25-4.0 mm。
|
‧ 僅能由受過適當訓練的醫師,執行支架置入。
‧ 僅可在可隨時進行緊急冠狀動脈繞道(CABG)手術的醫院,進行支架置入。
‧ 尚未評估新能吉支架與其他藥物釋放型或外覆型支架的潛在交互作用。
‧ 後續發生的血管再狹窄,可能需重複擴張含有支架的動脈區段。尚不清楚重複擴張冠狀動脈血管支架的長期結果。
‧ 對顯影劑具有嚴重反應病史的患者,應考量使用本裝置的風險與效益。
‧ 請勿讓支架傳送系統接觸到有機溶劑,如酒精或清潔劑。
‧ 支架傳送、展開及取出氣球時,應謹慎控制導引導管尖端的位置。在取出支架傳送系統(SDS)前,請透過螢光鏡目測確認氣球已完全消氣(請見表三、代表性系統消氣時間)。若未進行確認,可能會增加取出SDS所需的力道,並使導引導管在血管內移位及後續出現的動脈損傷。
‧ 同時口服艾諾莉茉斯及環孢素(cyclosporine),會使血清膽固醇及三酸甘油脂濃度上升。
|
在原生的冠狀動脈中使用冠狀動脈支架可能引起的副作用如下,包括經皮冠狀動脈擴張術及支架可能產生的風險:
突然支架閉合、急性心肌梗塞、過敏反應(包括抗凝血及抗血小板藥物治療,顯影劑,支架材質)、心絞痛、心律不整(包括心室纖維性顫動(VF)和心室性心動過速(VT))、動靜脈廔管、出血、心包膜填塞、心因性休克/肺水腫、冠狀動脈瘤、死亡、血管剝離、遠端栓塞(空氣、組織、血栓或使用於手術之器材的材料)、心衰竭、血腫、可能需要輸血的出血、低血壓/高血壓、局部或全身感染、心肌局部缺血、穿刺部位疼痛、冠狀動脈穿孔或破裂、心包積液(pericardial effusion)、股動脈假性血管瘤、腎功能不全或腎衰竭、呼吸衰竭、支架再狹窄、支架變形、支架栓塞或位移、支架斷裂、支架血栓形成/血管閉塞、中風/腦血管意外/暫時性(腦)缺血發作(TIA)、冠狀動脈完全閉塞、血管痙攣、需要進行外科的修復或重新進行介入性手術的血管損傷
|
NA
|
| 3.00-2.50*60拜歐邁茉福(冠狀)塗藥支架BIM30025060 |  | MERIL | $80,099.00 | $14,099.00 | $66,000.00 | |
1.為新型錐狀設計冠狀動脈塗藥支架系統。
2.市面上最長規格,避免治療風險,減少手術時間並減低病人療程費用。
3.以鈷鉻合金支架材質,使支架外擴更小,提升輸送能力及過彎力,提高手術成功率及手術室之使用率。
4.使用抗增殖藥物sirolimus(也稱Rapamycin), 快速進入血管壁,抑制內皮細胞過度增生,有效降低再阻塞率,維持血管暢通及病患術後良好之癒後。
5.承載藥物之聚合物,植入病患體內60天後降解完畢,能降低血栓之形成,提高病患安全性。
6.此新一代塗藥支架Biomime Morph,兼具有效性及安全性。
|
本產品用途為改善冠狀動脈管腔直徑,治療原發性冠狀動脈狹窄引起的缺血性心臟疾病,適用於有病狀且可接受經皮冠狀動脈形成術(PTCA),和支架置入術的患者(血管長度≦ 56mm ,直徑介於2.25mm 至 3.5mm)。
|
1.支架植入術只能在必要時能施行緊急冠狀動脈繞道手術。
2.支架植入術僅能由接受足夠培訓的醫生進行。
|
支架內血栓: 裝置塗藥支架後一個月內的發生率 <1%;晚期支架內血栓的發生率約0.5%(即使在6~12個月之後仍有可能發生)。
|
1.冠狀動脈塗藥支架置放後再狹窄率可降低至小於10%。
2.服用雙抗血小板藥物的時間較長(1年)。
|
| 3.50-3.00*60拜歐邁茉福(冠狀)塗藥支架BIM35030060 |  | MERIL | $80,099.00 | $14,099.00 | $66,000.00 | |
1.為新型錐狀設計冠狀動脈塗藥支架系統。
2.市面上最長規格,避免治療風險,減少手術時間並減低病人療程費用。
3.以鈷鉻合金支架材質,使支架外擴更小,提升輸送能力及過彎力,提高手術成功率及手術室之使用率。
4.使用抗增殖藥物sirolimus(也稱Rapamycin), 快速進入血管壁,抑制內皮細胞過度增生,有效降低再阻塞率,維持血管暢通及病患術後良好之癒後。
5.承載藥物之聚合物,植入病患體內60天後降解完畢,能降低血栓之形成,提高病患安全性。
6.此新一代塗藥支架Biomime Morph,兼具有效性及安全性。
|
本產品用途為改善冠狀動脈管腔直徑,治療原發性冠狀動脈狹窄引起的缺血性心臟疾病,適用於有病狀且可接受經皮冠狀動脈形成術(PTCA),和支架置入術的患者(血管長度≦ 56mm ,直徑介於2.25mm 至 3.5mm)。
|
1.支架植入術只能在必要時能施行緊急冠狀動脈繞道手術。
2.支架植入術僅能由接受足夠培訓的醫生進行。
|
支架內血栓: 裝置塗藥支架後一個月內的發生率 <1%;晚期支架內血栓的發生率約0.5%(即使在6~12個月之後仍有可能發生)。
|
1.冠狀動脈塗藥支架置放後再狹窄率可降低至小於10%。
2.服用雙抗血小板藥物的時間較長(1年)。
|
| 2.5*33mm那可米冠狀動脈塗藥支架系統DE-RS2533ASM |  | TERUMO | $74,099.00 | $14,099.00 | $60,000.00 | |
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶等病灶。
|
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶,65歲以上患者,男性或女性患者,完全阻塞病灶,長病灶,小血管病灶,再狹窄病灶包括支架內再挾窄,血管開口病灶,左主幹病灶及動靜脈繞道移植病灶。
|
1.本醫療器材只限由醫師操作使用
2.在透射攝影下操作
3.確認包裝沒有破損
|
突發性血管閉鎖,急性心肌梗塞,藥物過敏,動脈瘤,心律不整,支架內再狹窄,中風,血栓,發燒,心肌衰竭,出血,心絞痛,腎臟衰竭,心因性休克,死亡等。
|
1.支架再狹窄率低於健保支架
2.具有最長的尺寸,適用於病灶較長的情況下,不用置放2支支架
|
| 2.5*44mm可米冠狀動脈塗藥支架系統DE-RS2544ASM |  | TERUMO | $74,099.00 | $14,099.00 | $60,000.00 | |
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶等病灶。
|
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶,65歲以上患者,男性或女性患者,完全阻塞病灶,長病灶,小血管病灶,再狹窄病灶包括支架內再挾窄,血管開口病灶,左主幹病灶及動靜脈繞道移植病灶。
|
1.本醫療器材只限由醫師操作使用
2.在透射攝影下操作
3.確認包裝沒有破損
|
突發性血管閉鎖,急性心肌梗塞,藥物過敏,動脈瘤,心律不整,支架內再狹窄,中風,血栓,發燒,心肌衰竭,出血,心絞痛,腎臟衰竭,心因性休克,死亡等。
|
1.支架再狹窄率低於健保支架
2.具有最長的尺寸,適用於病灶較長的情況下,不用置放2支支架
|
| 2.5*50mm那可米冠狀動脈塗藥支架系統DE-RS2550ASM |  | TERUMO | $79,099.00 | $14,099.00 | $65,000.00 | |
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶等病灶。
|
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶,65歲以上患者,男性或女性患者,完全阻塞病灶,長病灶,小血管病灶,再狹窄病灶包括支架內再挾窄,血管開口病灶,左主幹病灶及動靜脈繞道移植病灶。
|
1.本醫療器材只限由醫師操作使用
2.在透射攝影下操作
3.確認包裝沒有破損
|
突發性血管閉鎖,急性心肌梗塞,藥物過敏,動脈瘤,心律不整,支架內再狹窄,中風,血栓,發燒,心肌衰竭,出血,心絞痛,腎臟衰竭,心因性休克,死亡等。
|
1.支架再狹窄率低於健保支架
2.具有最長的尺寸,適用於病灶較長的情況下,不用置放2支支架
|
| 2.75*33mm那可米冠狀動脈塗藥支架系統DE-RS2733ASM |  | TERUMO | $74,099.00 | $14,099.00 | $60,000.00 | |
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶等病灶。
|
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶,65歲以上患者,男性或女性患者,完全阻塞病灶,長病灶,小血管病灶,再狹窄病灶包括支架內再挾窄,血管開口病灶,左主幹病灶及動靜脈繞道移植病灶。
|
1.本醫療器材只限由醫師操作使用
2.在透射攝影下操作
3.確認包裝沒有破損
|
突發性血管閉鎖,急性心肌梗塞,藥物過敏,動脈瘤,心律不整,支架內再狹窄,中風,血栓,發燒,心肌衰竭,出血,心絞痛,腎臟衰竭,心因性休克,死亡等。
|
1.支架再狹窄率低於健保支架
2.具有最長的尺寸,適用於病灶較長的情況下,不用置放2支支架
|
| 2.75*44mm那可米冠狀動脈塗藥支架系統DE-RS2744ASM |  | TERUMO | $74,099.00 | $14,099.00 | $60,000.00 | |
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶等病灶。
|
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶,65歲以上患者,男性或女性患者,完全阻塞病灶,長病灶,小血管病灶,再狹窄病灶包括支架內再挾窄,血管開口病灶,左主幹病灶及動靜脈繞道移植病灶。
|
1.本醫療器材只限由醫師操作使用
2.在透射攝影下操作
3.確認包裝沒有破損
|
突發性血管閉鎖,急性心肌梗塞,藥物過敏,動脈瘤,心律不整,支架內再狹窄,中風,血栓,發燒,心肌衰竭,出血,心絞痛,腎臟衰竭,心因性休克,死亡等。
|
1.支架再狹窄率低於健保支架
2.具有最長的尺寸,適用於病灶較長的情況下,不用置放2支支架
|
| 2.75*50mm那可米冠狀動脈塗藥支架系統DE-RS2750ASM |  | TERUMO | $79,099.00 | $14,099.00 | $65,000.00 | |
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶等病灶。
|
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶,65歲以上患者,男性或女性患者,完全阻塞病灶,長病灶,小血管病灶,再狹窄病灶包括支架內再挾窄,血管開口病灶,左主幹病灶及動靜脈繞道移植病灶。
|
1.本醫療器材只限由醫師操作使用
2.在透射攝影下操作
3.確認包裝沒有破損
|
突發性血管閉鎖,急性心肌梗塞,藥物過敏,動脈瘤,心律不整,支架內再狹窄,中風,血栓,發燒,心肌衰竭,出血,心絞痛,腎臟衰竭,心因性休克,死亡等。
|
1.支架再狹窄率低於健保支架
2.具有最長的尺寸,適用於病灶較長的情況下,不用置放2支支架
|
| 3.0*33mm可米冠狀動脈塗藥支架系統DE-RS3033ASM |  | TERUMO | $74,099.00 | $14,099.00 | $60,000.00 | |
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶等病灶。
|
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶,65歲以上患者,男性或女性患者,完全阻塞病灶,長病灶,小血管病灶,再狹窄病灶包括支架內再挾窄,血管開口病灶,左主幹病灶及動靜脈繞道移植病灶。
|
1.本醫療器材只限由醫師操作使用
2.在透射攝影下操作
3.確認包裝沒有破損
|
突發性血管閉鎖,急性心肌梗塞,藥物過敏,動脈瘤,心律不整,支架內再狹窄,中風,血栓,發燒,心肌衰竭,出血,心絞痛,腎臟衰竭,心因性休克,死亡等。
|
1.支架再狹窄率低於健保支架
2.具有最長的尺寸,適用於病灶較長的情況下,不用置放2支支架
|
| 3.0*44mm那可米冠狀動脈塗藥支架系統DE-RS3044ASM |  | TERUMO | $74,099.00 | $14,099.00 | $60,000.00 | |
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶等病灶。
|
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶,65歲以上患者,男性或女性患者,完全阻塞病灶,長病灶,小血管病灶,再狹窄病灶包括支架內再挾窄,血管開口病灶,左主幹病灶及動靜脈繞道移植病灶。
|
1.本醫療器材只限由醫師操作使用
2.在透射攝影下操作
3.確認包裝沒有破損
|
突發性血管閉鎖,急性心肌梗塞,藥物過敏,動脈瘤,心律不整,支架內再狹窄,中風,血栓,發燒,心肌衰竭,出血,心絞痛,腎臟衰竭,心因性休克,死亡等。
|
1.支架再狹窄率低於健保支架
2.具有最長的尺寸,適用於病灶較長的情況下,不用置放2支支架
|
| 3.0*50mm那可米冠狀動脈塗藥支架系統DE-RS3050ASM |  | TERUMO | $79,099.00 | $14,099.00 | $65,000.00 | |
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶等病灶。
|
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶,65歲以上患者,男性或女性患者,完全阻塞病灶,長病灶,小血管病灶,再狹窄病灶包括支架內再挾窄,血管開口病灶,左主幹病灶及動靜脈繞道移植病灶。
|
1.本醫療器材只限由醫師操作使用
2.在透射攝影下操作
3.確認包裝沒有破損
|
突發性血管閉鎖,急性心肌梗塞,藥物過敏,動脈瘤,心律不整,支架內再狹窄,中風,血栓,發燒,心肌衰竭,出血,心絞痛,腎臟衰竭,心因性休克,死亡等。
|
1.支架再狹窄率低於健保支架
2.具有最長的尺寸,適用於病灶較長的情況下,不用置放2支支架
|
| 3.5*33mm那可米冠狀動脈塗藥支架系統DE-RS3533ASM |  | TERUMO | $74,099.00 | $14,099.00 | $60,000.00 | |
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶等病灶。
|
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶,65歲以上患者,男性或女性患者,完全阻塞病灶,長病灶,小血管病灶,再狹窄病灶包括支架內再挾窄,血管開口病灶,左主幹病灶及動靜脈繞道移植病灶。
|
1.本醫療器材只限由醫師操作使用
2.在透射攝影下操作
3.確認包裝沒有破損
|
突發性血管閉鎖,急性心肌梗塞,藥物過敏,動脈瘤,心律不整,支架內再狹窄,中風,血栓,發燒,心肌衰竭,出血,心絞痛,腎臟衰竭,心因性休克,死亡等。
|
1.支架再狹窄率低於健保支架
2.具有最長的尺寸,適用於病灶較長的情況下,不用置放2支支架
|
| 3.5*44mm那可米冠狀動脈塗藥支架系統DE-RS3544ASM |  | TERUMO | $74,099.00 | $14,099.00 | $60,000.00 | |
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶等病灶。
|
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶,65歲以上患者,男性或女性患者,完全阻塞病灶,長病灶,小血管病灶,再狹窄病灶包括支架內再挾窄,血管開口病灶,左主幹病灶及動靜脈繞道移植病灶。
|
1.本醫療器材只限由醫師操作使用
2.在透射攝影下操作
3.確認包裝沒有破損
|
突發性血管閉鎖,急性心肌梗塞,藥物過敏,動脈瘤,心律不整,支架內再狹窄,中風,血栓,發燒,心肌衰竭,出血,心絞痛,腎臟衰竭,心因性休克,死亡等。
|
1.支架再狹窄率低於健保支架
2.具有最長的尺寸,適用於病灶較長的情況下,不用置放2支支架
|
| 3.5*50mm那可米冠狀動脈塗藥支架系統DE-RS3550ASM |  | TERUMO | $79,099.00 | $14,099.00 | $65,000.00 | |
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶等病灶。
|
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶,65歲以上患者,男性或女性患者,完全阻塞病灶,長病灶,小血管病灶,再狹窄病灶包括支架內再挾窄,血管開口病灶,左主幹病灶及動靜脈繞道移植病灶。
|
1.本醫療器材只限由醫師操作使用
2.在透射攝影下操作
3.確認包裝沒有破損
|
突發性血管閉鎖,急性心肌梗塞,藥物過敏,動脈瘤,心律不整,支架內再狹窄,中風,血栓,發燒,心肌衰竭,出血,心絞痛,腎臟衰竭,心因性休克,死亡等。
|
1.支架再狹窄率低於健保支架
2.具有最長的尺寸,適用於病灶較長的情況下,不用置放2支支架
|
| 4.0*33mm那可米冠狀動脈塗藥支架系統DE-RS4033ASM |  | TERUMO | $74,099.00 | $14,099.00 | $60,000.00 | |
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶等病灶。
|
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶,65歲以上患者,男性或女性患者,完全阻塞病灶,長病灶,小血管病灶,再狹窄病灶包括支架內再挾窄,血管開口病灶,左主幹病灶及動靜脈繞道移植病灶。
|
1.本醫療器材只限由醫師操作使用
2.在透射攝影下操作
3.確認包裝沒有破損
|
突發性血管閉鎖,急性心肌梗塞,藥物過敏,動脈瘤,心律不整,支架內再狹窄,中風,血栓,發燒,心肌衰竭,出血,心絞痛,腎臟衰竭,心因性休克,死亡等。
|
1.支架再狹窄率低於健保支架
2.具有最長的尺寸,適用於病灶較長的情況下,不用置放2支支架
|
| 4.0*44mm那可米冠狀動脈塗藥支架系統DE-RS4044ASM |  | TERUMO | $74,099.00 | $14,099.00 | $60,000.00 | |
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶等病灶。
|
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶,65歲以上患者,男性或女性患者,完全阻塞病灶,長病灶,小血管病灶,再狹窄病灶包括支架內再挾窄,血管開口病灶,左主幹病灶及動靜脈繞道移植病灶。
|
1.本醫療器材只限由醫師操作使用
2.在透射攝影下操作
3.確認包裝沒有破損
|
突發性血管閉鎖,急性心肌梗塞,藥物過敏,動脈瘤,心律不整,支架內再狹窄,中風,血栓,發燒,心肌衰竭,出血,心絞痛,腎臟衰竭,心因性休克,死亡等。
|
1.支架再狹窄率低於健保支架
2.具有最長的尺寸,適用於病灶較長的情況下,不用置放2支支架
|
| 4.0*50mm那可米冠狀動脈塗藥支架系統DE-RS4050ASM |  | TERUMO | $79,099.00 | $14,099.00 | $65,000.00 | |
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶等病灶。
|
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶,65歲以上患者,男性或女性患者,完全阻塞病灶,長病灶,小血管病灶,再狹窄病灶包括支架內再挾窄,血管開口病灶,左主幹病灶及動靜脈繞道移植病灶。
|
1.本醫療器材只限由醫師操作使用
2.在透射攝影下操作
3.確認包裝沒有破損
|
突發性血管閉鎖,急性心肌梗塞,藥物過敏,動脈瘤,心律不整,支架內再狹窄,中風,血栓,發燒,心肌衰竭,出血,心絞痛,腎臟衰竭,心因性休克,死亡等。
|
1.支架再狹窄率低於健保支架
2.具有最長的尺寸,適用於病灶較長的情況下,不用置放2支支架
|
| 2.5*21mm那可米冠狀動脈塗藥支架系統DE-RS2521ASM |  | TERUMO | $74,099.00 | $14,099.00 | $60,000.00 | |
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶等病灶。
|
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶,65歲以上患者,男性或女性患者,完全阻塞病灶,長病灶,小血管病灶,再狹窄病灶包括支架內再挾窄,血管開口病灶,左主幹病灶及動靜脈繞道移植病灶。
|
1.本醫療器材只限由醫師操作使用
2.在透射攝影下操作
3.確認包裝沒有破損
|
突發性血管閉鎖,急性心肌梗塞,藥物過敏,動脈瘤,心律不整,支架內再狹窄,中風,血栓,發燒,心肌衰竭,出血,心絞痛,腎臟衰竭,心因性休克,死亡等。
|
1.支架再狹窄率低於健保支架
2.具有最長的尺寸,適用於病灶較長的情況下,不用置放2支支架
|
| 2.5*24mm那可米冠狀動脈塗藥支架系統DE-RS2524ASM |  | TERUMO | $74,099.00 | $14,099.00 | $60,000.00 | |
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶等病灶。
|
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶,65歲以上患者,男性或女性患者,完全阻塞病灶,長病灶,小血管病灶,再狹窄病灶包括支架內再挾窄,血管開口病灶,左主幹病灶及動靜脈繞道移植病灶。
|
1.本醫療器材只限由醫師操作使用
2.在透射攝影下操作
3.確認包裝沒有破損
|
突發性血管閉鎖,急性心肌梗塞,藥物過敏,動脈瘤,心律不整,支架內再狹窄,中風,血栓,發燒,心肌衰竭,出血,心絞痛,腎臟衰竭,心因性休克,死亡等。
|
1.支架再狹窄率低於健保支架
2.具有最長的尺寸,適用於病灶較長的情況下,不用置放2支支架
|
| 2.5*28mm那可米冠狀動脈塗藥支架系統DE-RS2528ASM |  | TERUMO | $74,099.00 | $14,099.00 | $60,000.00 | |
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶等病灶。
|
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶,65歲以上患者,男性或女性患者,完全阻塞病灶,長病灶,小血管病灶,再狹窄病灶包括支架內再挾窄,血管開口病灶,左主幹病灶及動靜脈繞道移植病灶。
|
1.本醫療器材只限由醫師操作使用
2.在透射攝影下操作
3.確認包裝沒有破損
|
突發性血管閉鎖,急性心肌梗塞,藥物過敏,動脈瘤,心律不整,支架內再狹窄,中風,血栓,發燒,心肌衰竭,出血,心絞痛,腎臟衰竭,心因性休克,死亡等。
|
1.支架再狹窄率低於健保支架
2.具有最長的尺寸,適用於病灶較長的情況下,不用置放2支支架
|
| 2.75*21mm那可米冠狀動脈塗藥支架系統DE-RS2721ASM |  | TERUMO | $74,099.00 | $14,099.00 | $60,000.00 | |
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶等病灶。
|
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶,65歲以上患者,男性或女性患者,完全阻塞病灶,長病灶,小血管病灶,再狹窄病灶包括支架內再挾窄,血管開口病灶,左主幹病灶及動靜脈繞道移植病灶。
|
1.本醫療器材只限由醫師操作使用
2.在透射攝影下操作
3.確認包裝沒有破損
|
突發性血管閉鎖,急性心肌梗塞,藥物過敏,動脈瘤,心律不整,支架內再狹窄,中風,血栓,發燒,心肌衰竭,出血,心絞痛,腎臟衰竭,心因性休克,死亡等。
|
1.支架再狹窄率低於健保支架
2.具有最長的尺寸,適用於病灶較長的情況下,不用置放2支支架
|
| 2.75*24mm那可米冠狀動脈塗藥支架系統DE-RS2724ASM |  | TERUMO | $74,099.00 | $14,099.00 | $60,000.00 | |
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶等病灶。
|
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶,65歲以上患者,男性或女性患者,完全阻塞病灶,長病灶,小血管病灶,再狹窄病灶包括支架內再挾窄,血管開口病灶,左主幹病灶及動靜脈繞道移植病灶。
|
1.本醫療器材只限由醫師操作使用
2.在透射攝影下操作
3.確認包裝沒有破損
|
突發性血管閉鎖,急性心肌梗塞,藥物過敏,動脈瘤,心律不整,支架內再狹窄,中風,血栓,發燒,心肌衰竭,出血,心絞痛,腎臟衰竭,心因性休克,死亡等。
|
1.支架再狹窄率低於健保支架
2.具有最長的尺寸,適用於病灶較長的情況下,不用置放2支支架
|
| 2.75*28mm那可米冠狀動脈塗藥支架系統DE-RS2728ASM |  | TERUMO | $74,099.00 | $14,099.00 | $60,000.00 | |
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶等病灶。
|
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶,65歲以上患者,男性或女性患者,完全阻塞病灶,長病灶,小血管病灶,再狹窄病灶包括支架內再挾窄,血管開口病灶,左主幹病灶及動靜脈繞道移植病灶。
|
1.本醫療器材只限由醫師操作使用
2.在透射攝影下操作
3.確認包裝沒有破損
|
突發性血管閉鎖,急性心肌梗塞,藥物過敏,動脈瘤,心律不整,支架內再狹窄,中風,血栓,發燒,心肌衰竭,出血,心絞痛,腎臟衰竭,心因性休克,死亡等。
|
1.支架再狹窄率低於健保支架
2.具有最長的尺寸,適用於病灶較長的情況下,不用置放2支支架
|
| 3.0*21mm那可米冠狀動脈塗藥支架系統DE-RS3021ASM |  | TERUMO | $74,099.00 | $14,099.00 | $60,000.00 | |
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶等病灶。
|
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶,65歲以上患者,男性或女性患者,完全阻塞病灶,長病灶,小血管病灶,再狹窄病灶包括支架內再挾窄,血管開口病灶,左主幹病灶及動靜脈繞道移植病灶。
|
1.本醫療器材只限由醫師操作使用
2.在透射攝影下操作
3.確認包裝沒有破損
|
突發性血管閉鎖,急性心肌梗塞,藥物過敏,動脈瘤,心律不整,支架內再狹窄,中風,血栓,發燒,心肌衰竭,出血,心絞痛,腎臟衰竭,心因性休克,死亡等。
|
1.支架再狹窄率低於健保支架
2.具有最長的尺寸,適用於病灶較長的情況下,不用置放2支支架
|
| 3.0*24mm那可米冠狀動脈塗藥支架系統DE-RS3024ASM |  | TERUMO | $74,099.00 | $14,099.00 | $60,000.00 | |
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶等病灶。
|
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶,65歲以上患者,男性或女性患者,完全阻塞病灶,長病灶,小血管病灶,再狹窄病灶包括支架內再挾窄,血管開口病灶,左主幹病灶及動靜脈繞道移植病灶。
|
1.本醫療器材只限由醫師操作使用
2.在透射攝影下操作
3.確認包裝沒有破損
|
突發性血管閉鎖,急性心肌梗塞,藥物過敏,動脈瘤,心律不整,支架內再狹窄,中風,血栓,發燒,心肌衰竭,出血,心絞痛,腎臟衰竭,心因性休克,死亡等。
|
1.支架再狹窄率低於健保支架
2.具有最長的尺寸,適用於病灶較長的情況下,不用置放2支支架
|
| 3.0*28mm那可米冠狀動脈塗藥支架系統DE-RS3028ASM |  | TERUMO | $74,099.00 | $14,099.00 | $60,000.00 | |
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶等病灶。
|
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶,65歲以上患者,男性或女性患者,完全阻塞病灶,長病灶,小血管病灶,再狹窄病灶包括支架內再挾窄,血管開口病灶,左主幹病灶及動靜脈繞道移植病灶。
|
1.本醫療器材只限由醫師操作使用
2.在透射攝影下操作
3.確認包裝沒有破損
|
突發性血管閉鎖,急性心肌梗塞,藥物過敏,動脈瘤,心律不整,支架內再狹窄,中風,血栓,發燒,心肌衰竭,出血,心絞痛,腎臟衰竭,心因性休克,死亡等。
|
1.支架再狹窄率低於健保支架
2.具有最長的尺寸,適用於病灶較長的情況下,不用置放2支支架
|
| 3.5*21mm那可米冠狀動脈塗藥支架系統DE-RS3521ASM |  | TERUMO | $74,099.00 | $14,099.00 | $60,000.00 | |
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶等病灶。
|
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶,65歲以上患者,男性或女性患者,完全阻塞病灶,長病灶,小血管病灶,再狹窄病灶包括支架內再挾窄,血管開口病灶,左主幹病灶及動靜脈繞道移植病灶。
|
1.本醫療器材只限由醫師操作使用
2.在透射攝影下操作
3.確認包裝沒有破損
|
突發性血管閉鎖,急性心肌梗塞,藥物過敏,動脈瘤,心律不整,支架內再狹窄,中風,血栓,發燒,心肌衰竭,出血,心絞痛,腎臟衰竭,心因性休克,死亡等。
|
1.支架再狹窄率低於健保支架
2.具有最長的尺寸,適用於病灶較長的情況下,不用置放2支支架
|
| 3.5*24mm那可米冠狀動脈塗藥支架系統DE-RS3524ASM |  | TERUMO | $74,099.00 | $14,099.00 | $60,000.00 | |
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶等病灶。
|
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶,65歲以上患者,男性或女性患者,完全阻塞病灶,長病灶,小血管病灶,再狹窄病灶包括支架內再挾窄,血管開口病灶,左主幹病灶及動靜脈繞道移植病灶。
|
1.本醫療器材只限由醫師操作使用
2.在透射攝影下操作
3.確認包裝沒有破損
|
突發性血管閉鎖,急性心肌梗塞,藥物過敏,動脈瘤,心律不整,支架內再狹窄,中風,血栓,發燒,心肌衰竭,出血,心絞痛,腎臟衰竭,心因性休克,死亡等。
|
1.支架再狹窄率低於健保支架
2.具有最長的尺寸,適用於病灶較長的情況下,不用置放2支支架
|
| 3.5*28mm那可米冠狀動脈塗藥支架系統DE-RS3528ASM |  | TERUMO | $74,099.00 | $14,099.00 | $60,000.00 | |
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶等病灶。
|
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶,65歲以上患者,男性或女性患者,完全阻塞病灶,長病灶,小血管病灶,再狹窄病灶包括支架內再挾窄,血管開口病灶,左主幹病灶及動靜脈繞道移植病灶。
|
1.本醫療器材只限由醫師操作使用
2.在透射攝影下操作
3.確認包裝沒有破損
|
突發性血管閉鎖,急性心肌梗塞,藥物過敏,動脈瘤,心律不整,支架內再狹窄,中風,血栓,發燒,心肌衰竭,出血,心絞痛,腎臟衰竭,心因性休克,死亡等。
|
1.支架再狹窄率低於健保支架
2.具有最長的尺寸,適用於病灶較長的情況下,不用置放2支支架
|
| 4.0*21mm那可米冠狀動脈塗藥支架系統DE-RS4021ASM |  | TERUMO | $74,099.00 | $14,099.00 | $60,000.00 | |
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶等病灶。
|
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶,65歲以上患者,男性或女性患者,完全阻塞病灶,長病灶,小血管病灶,再狹窄病灶包括支架內再挾窄,血管開口病灶,左主幹病灶及動靜脈繞道移植病灶。
|
1.本醫療器材只限由醫師操作使用
2.在透射攝影下操作
3.確認包裝沒有破損
|
突發性血管閉鎖,急性心肌梗塞,藥物過敏,動脈瘤,心律不整,支架內再狹窄,中風,血栓,發燒,心肌衰竭,出血,心絞痛,腎臟衰竭,心因性休克,死亡等。
|
1.支架再狹窄率低於健保支架
2.具有最長的尺寸,適用於病灶較長的情況下,不用置放2支支架
|
| 4.0*24mm那可米冠狀動脈塗藥支架系統DE-RS4024ASM |  | TERUMO | $74,099.00 | $14,099.00 | $60,000.00 | |
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶等病灶。
|
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶,65歲以上患者,男性或女性患者,完全阻塞病灶,長病灶,小血管病灶,再狹窄病灶包括支架內再挾窄,血管開口病灶,左主幹病灶及動靜脈繞道移植病灶。
|
1.本醫療器材只限由醫師操作使用
2.在透射攝影下操作
3.確認包裝沒有破損
|
突發性血管閉鎖,急性心肌梗塞,藥物過敏,動脈瘤,心律不整,支架內再狹窄,中風,血栓,發燒,心肌衰竭,出血,心絞痛,腎臟衰竭,心因性休克,死亡等。
|
1.支架再狹窄率低於健保支架
2.具有最長的尺寸,適用於病灶較長的情況下,不用置放2支支架
|
| 4.0*28mm那可米冠狀動脈塗藥支架系統DE-RS4028ASM |  | TERUMO | $74,099.00 | $14,099.00 | $60,000.00 | |
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶等病灶。
|
用於治療患者冠狀動脈狹窄或阻塞型病灶,包括但不限於慢性冠心症,急性冠心症,糖尿病,多條血管疾病,分叉病灶,65歲以上患者,男性或女性患者,完全阻塞病灶,長病灶,小血管病灶,再狹窄病灶包括支架內再挾窄,血管開口病灶,左主幹病灶及動靜脈繞道移植病灶。
|
1.本醫療器材只限由醫師操作使用
2.在透射攝影下操作
3.確認包裝沒有破損
|
突發性血管閉鎖,急性心肌梗塞,藥物過敏,動脈瘤,心律不整,支架內再狹窄,中風,血栓,發燒,心肌衰竭,出血,心絞痛,腎臟衰竭,心因性休克,死亡等。
|
1.支架再狹窄率低於健保支架
2.具有最長的尺寸,適用於病灶較長的情況下,不用置放2支支架
|
| 42866 抗虹吸及可調式二合一控制閥 |  | MEDTRONIC | $70,000.00 | $7,127.00 | $62,873.00 |  品項用途 品項用途 |
在移植手術後,“美敦力”Strata II控制閥提供了一項非侵入的方式,以符合病患在水腦症控制上不同的需求。藉由控制閥的特殊設計,讓醫師們可以使用PS Medical Strata 控制閥調整組來調整控制閥壓力/功效等級。此一設計有助於當控制閥遇到偶發性變化時,讓其功效等級維持不變。
Strata II控制閥是由一球形和一錐形壓力控制閥系列,及於常態下通常為關閉狀態的虹吸控制機制(Delta chamber)所組成。不論病患的身體姿勢或腦脊髓液流速需求為何,此組合讓控制閥得以將腦室內壓維持在正常生理範圍內。流速管制則是由球形和錐形壓力控制閥和虹吸控制膈膜合力完成。控制閥的功效特色取決於阻力的大小。球形及錐形壓力控制閥可以避免CSF逆流。虹吸作用則由Delta charnber的兩片矽質彈性膈膜所控制,該隔膜於常態下為關閉的狀態。若遇到逆向的腦室內壓,兩片膈膜就會打開。
小型或一般型Strata II控制閥可以提供一系列的功效等級:0.5、1.0、1.5、2.0,及 2.5。
|
“美敦力”Strata II控制閥是一引流組件之一,其設計是為了將持續的腦脊髓液從腦室引流入右心房或腹膜腔。Strata II控制閥讓醫師能以非侵入的方式,來調整壓力/流速的功效等級,無論在植入前或植入後不含X光攝影確認的需要,皆為了符合病患需求的改變。
|
禁忌症:
如果任何引流系統組件的植入部位有感染存在,引流腦脊髓液至腹腔或身體其他部位不應進行。這包括頭皮與其他引流系統途經之皮膚、腦膜、腦室、腹膜/腹膜內/後腹腔器官、胸膜、與血液系統。當身體任一部位發生感染,禁止進行腦脊髓液引流。再者,如病患患有先天性心臟病或其他嚴重心肺異常,禁止引流到心房。
|
目前無臨床或研究顯示其副作用。
|
無健保已給付項目
|
| 2.5x22mm歐德邁冠狀動脈支架系統LICM25-22OPTI |  | HEXACATH | $72,099.00 | $14,099.00 | $58,000.00 | |
全民健保保險給付第三類別特殊塗層支架 材質為雷射裁切鈷珞合金並塗有氮氧化鈦塗層,彈性管狀支架
|
急性冠狀動脈症候群(ACS)的原始的或緊急的血管成形術
|
傳統成形術必須使用動脈導引鞘,導引導管與導線 , 內徑0.58”(1.47mm)的5F導引導管可用來推進直徑2.0mm至4.0mm的本產品,內徑0.64”(1.62mm)導引導管可用來推進直徑4.5mm至5.0mm的本產品
|
感染出血/血腫栓塞血栓冠狀動脈痙攣冠狀動脈病灶(撕裂、穿孔、破裂)動靜脈?管已擴張動脈再狹窄化已擴張動脈完全閉塞高血壓不穩定性心絞痛心律不整,包括心室纖維性顫動急性心肌梗塞
|
2 目標病灶再阻塞比健保支架及塗藥支架低
|
| 2.5x28mm歐德邁冠狀動脈支架系統LICM25-28OPTI |  | HEXACATH | $72,099.00 | $14,099.00 | $58,000.00 | |
全民健保保險給付第三類別特殊塗層支架 材質為雷射裁切鈷珞合金並塗有氮氧化鈦塗層,彈性管狀支架
|
急性冠狀動脈症候群(ACS)的原始的或緊急的血管成形術
|
傳統成形術必須使用動脈導引鞘,導引導管與導線 , 內徑0.58”(1.47mm)的5F導引導管可用來推進直徑2.0mm至4.0mm的本產品,內徑0.64”(1.62mm)導引導管可用來推進直徑4.5mm至5.0mm的本產品
|
感染出血/血腫栓塞血栓冠狀動脈痙攣冠狀動脈病灶(撕裂、穿孔、破裂)動靜脈?管已擴張動脈再狹窄化已擴張動脈完全閉塞高血壓不穩定性心絞痛心律不整,包括心室纖維性顫動急性心肌梗塞
|
4 心因性死亡發生比健保支架及塗藥支架低
|
| 2.75x16mm歐德邁冠狀動脈支架系統LICM275-16OPTI |  | HEXACATH | $72,099.00 | $14,099.00 | $58,000.00 | |
全民健保保險給付第三類別特殊塗層支架 材質為雷射裁切鈷珞合金並塗有氮氧化鈦塗層,彈性管狀支架
|
急性冠狀動脈症候群(ACS)的原始的或緊急的血管成形術
|
傳統成形術必須使用動脈導引鞘,導引導管與導線 , 內徑0.58”(1.47mm)的5F導引導管可用來推進直徑2.0mm至4.0mm的本產品,內徑0.64”(1.62mm)導引導管可用來推進直徑4.5mm至5.0mm的本產品
|
感染出血/血腫栓塞血栓冠狀動脈痙攣冠狀動脈病灶(撕裂、穿孔、破裂)動靜脈?管已擴張動脈再狹窄化已擴張動脈完全閉塞高血壓不穩定性心絞痛心律不整,包括心室纖維性顫動急性心肌梗塞
|
1 支架血栓發生比健保支架及塗藥支架低
|
| 2.75x22mm歐德邁冠狀動脈支架系統LICM275-22OPTI |  | HEXACATH | $72,099.00 | $14,099.00 | $58,000.00 | |
全民健保保險給付第三類別特殊塗層支架 材質為雷射裁切鈷珞合金並塗有氮氧化鈦塗層,彈性管狀支架
|
急性冠狀動脈症候群(ACS)的原始的或緊急的血管成形術
|
傳統成形術必須使用動脈導引鞘,導引導管與導線 , 內徑0.58”(1.47mm)的5F導引導管可用來推進直徑2.0mm至4.0mm的本產品,內徑0.64”(1.62mm)導引導管可用來推進直徑4.5mm至5.0mm的本產品
|
感染出血/血腫栓塞血栓冠狀動脈痙攣冠狀動脈病灶(撕裂、穿孔、破裂)動靜脈?管已擴張動脈再狹窄化已擴張動脈完全閉塞高血壓不穩定性心絞痛心律不整,包括心室纖維性顫動急性心肌梗塞
|
3 心肌梗塞再發生比健保支架及塗藥支架低
|
| 2.75x25mm歐德邁冠狀動脈支架系統LICM275-25OPTI |  | HEXACATH | $72,099.00 | $14,099.00 | $58,000.00 | |
全民健保保險給付第三類別特殊塗層支架 材質為雷射裁切鈷珞合金並塗有氮氧化鈦塗層,彈性管狀支架
|
急性冠狀動脈症候群(ACS)的原始的或緊急的血管成形術
|
傳統成形術必須使用動脈導引鞘,導引導管與導線 , 內徑0.58”(1.47mm)的5F導引導管可用來推進直徑2.0mm至4.0mm的本產品,內徑0.64”(1.62mm)導引導管可用來推進直徑4.5mm至5.0mm的本產品
|
感染出血/血腫栓塞血栓冠狀動脈痙攣冠狀動脈病灶(撕裂、穿孔、破裂)動靜脈?管已擴張動脈再狹窄化已擴張動脈完全閉塞高血壓不穩定性心絞痛心律不整,包括心室纖維性顫動急性心肌梗塞
|
4 心因性死亡發生比健保支架及塗藥支架低
|
| 3.0x32mm歐德邁冠狀動脈支架系統LICM30-32OPTI |  | HEXACATH | $72,099.00 | $14,099.00 | $58,000.00 | |
全民健保保險給付第三類別特殊塗層支架 材質為雷射裁切鈷珞合金並塗有氮氧化鈦塗層,彈性管狀支架
|
急性冠狀動脈症候群(ACS)的原始的或緊急的血管成形術
|
傳統成形術必須使用動脈導引鞘,導引導管與導線 , 內徑0.58”(1.47mm)的5F導引導管可用來推進直徑2.0mm至4.0mm的本產品,內徑0.64”(1.62mm)導引導管可用來推進直徑4.5mm至5.0mm的本產品
|
感染出血/血腫栓塞血栓冠狀動脈痙攣冠狀動脈病灶(撕裂、穿孔、破裂)動靜脈?管已擴張動脈再狹窄化已擴張動脈完全閉塞高血壓不穩定性心絞痛心律不整,包括心室纖維性顫動急性心肌梗塞
|
2 目標病灶再阻塞比健保支架及塗藥支架低
|
| RONYX40034X RESOLUTE ONYX 4.0MMX34MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX40034X RESOLUTE ONYX 4.0MMX34MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX40026X RESOLUTE ONYX 4.0MMX26MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
1.隔離不同的組織及防止傷疤組織向內生長,並防止緊靠阻黏膜部分的組織形成重新形成黏連。
2.促成緊靠阻黏膜的組織形成手術的解剖面,有助於手術再次的進行。
3.防止緊靠阻黏膜部分的形成或重新形成黏連,並促成緊靠阻黏膜的組織形成便於進行手術的解剖面。
4.增強軟組織的薄弱部位,或用於需要附加使用其它增強或搭橋材料才能達成期望的手術效果的疝氣或筋膜修補手術,用於需要臨時傷口支托的場合。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX40026X RESOLUTE ONYX 4.0MMX26MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
1.隔離不同的組織及防止傷疤組織向內生長,並防止緊靠阻黏膜部分的組織形成重新形成黏連。
2.促成緊靠阻黏膜的組織形成手術的解剖面,有助於手術再次的進行。
3.防止緊靠阻黏膜部分的形成或重新形成黏連,並促成緊靠阻黏膜的組織形成便於進行手術的解剖面。
4.增強軟組織的薄弱部位,或用於需要附加使用其它增強或搭橋材料才能達成期望的手術效果的疝氣或筋膜修補手術,用於需要臨時傷口支托的場合。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX40022X RESOLUTE INTEGRITY 4.0MMX22MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX40022X RESOLUTE INTEGRITY 4.0MMX22MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX35034X RESOLUTE ONYX 3.5MMX34MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX35034X RESOLUTE ONYX 3.5MMX34MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX35026X RESOLUTE ONYX 3.5MMX26MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX35026X RESOLUTE ONYX 3.5MMX26MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX35022X RESOLUTE ONYX 3.5MMX22MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX35022X RESOLUTE ONYX 3.5MMX22MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX30034X RESOLUTE ONYX 3.0MMX34MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX30026X RESOLUTE ONYX 3.0MMX26MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX30022X RESOLUTE ONYX 3.0MMX22MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX27526X RESOLUTE ONYX 2.75MMX26MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX27522X RESOLUTE ONYX 2.75MMX22MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX27534X Resolute Onyx 2.75MMX34MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX27538X Resolute Onyx 2.75MMX38MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX25026X RESOLUTE ONYX 2.5MMX26MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX25022X RESOLUTE ONYX 2.5MMX22MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX25034X Resolute Onyx 2.5MMX34MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX25038X Resolute Onyx 2.5MMX38MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX22526X RESOLUTE ONYX 2.25MMX26MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX22522X RESOLUTE ONYX 2.25MMX22MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX22515X Resolute Onyx 2.25MMx15MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 |  品項用途 品項用途 |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX22534X Resolute Onyx 2.25MMx34MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 |  品項用途 品項用途 |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX22538X RESOLUTE ONYX 2.25MMx38MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 |  品項用途 品項用途 |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX22518X RESOLUTE ONYX 2.25MMx18MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 |  品項用途 品項用途 |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX27512X RESOLUTE ONYX 2.75MMX12MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 |  品項用途 品項用途 |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX22530X RESOLUTE ONYX 2.25MMx30MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 |  品項用途 品項用途 |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX25015X RESOLUTE ONYX 2.5MMx15MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 |  品項用途 品項用途 |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX25018X RESOLUTE ONYX 2.5MMx18MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX25030X RESOLUTE ONYX 2.5MMx30MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX27515X RESOLUTE ONYX 2.75MMx15MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX27518X RESOLUTE ONYX 2.75MMx18MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX27530X RESOLUTE ONYX 2.75MMx30MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX30008X RESOLUTE ONYX 3.0MMx8MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX30012X RESOLUTE ONYX 3.0MMx12MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX30015X RESOLUTE ONYX 3.0MMx15MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX30018X RESOLUTE ONYX 3.0MMx18MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX30030X RESOLUTE ONYX 3.0MMx30MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX35008X RESOLUTE ONYX 3.5MMx8MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX35012X RESOLUTE ONYX 3.5MMx12MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX35015X RESOLUTE ONYX 3.5MMx15MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX35018X RESOLUTE ONYX 3.5MMx18MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX35030X RESOLUTE ONYX 3.5MMx30MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX40008X RESOLUTE ONYX 4.0MMx8MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX40012X RESOLUTE ONYX 4.0MMx12MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX40015X RESOLUTE ONYX 4.0MMx15MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX40018X RESOLUTE ONYX 4.0MMx18MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX40030X RESOLUTE ONYX 4.0MMx30MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX30038X RESOLUTE ONYX 3.0MMx38MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX35038X RESOLUTE ONYX 3.5MMx38MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX40038X RESOLUTE ONYX 4.0MMx38MM |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| 828805柯特曼史特斯引流閥--附配件(導管及具抗虹吸) |  | MEDOS | $113,400.00 | $7,127.00 | $106,273.00 | |
本產品為單次使用的可植入裝置,專供腦積水治療的腦脊髓液(CSF)分流之用。此閥門可進行八種不同的設定,以提供穩定的顱內壓與腦脊髓液引流。閥門的壓力會於術前設定,並可透過治療管理系統,亦即「TMS」進行非侵入性變更。此外附加的Siphonguard裝置可避免分流系統進行過度的腦脊髓液引流。
|
水腦症
|
本醫療器材只限由醫師操作使用
|
這些裝置嚴禁使用於接受抗凝血劑治療或已知具有易流血體質的患者若患者體內出現感染現象,請避免植入分流器。出現感染症狀時,如:腦膜炎,腦室炎,腹膜炎,菌血症及敗血病時,請延後分流器的植入手術。
|
此閥門可進行八種不同的設定,以提供穩定的顱內壓與腦脊髓液引流。閥門的壓力會於術前設定,並可透過治療管理系統,亦即「TMS」進行非侵入性變更。此外附加的Siphonguard裝置可避免分流系統進行過度的腦脊髓液引流。
|
| RONYX-200-15-X冠狀動脈塗藥支架(律動歐尼克斯) |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX-200-18-X冠狀動脈塗藥支架系統(律動歐尼克斯) |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX-200-22-X冠狀動脈塗藥支架系統(律動歐尼克斯) |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX-200-26-X冠狀動脈塗藥支架系統(律動歐尼克斯) |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX-200-30-X冠狀動脈塗藥支架系統(律動歐尼克斯) |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 搭載獨家製程CST專利設計,增加支架過彎靈活性及血管順應性,不影響血管原本構型造成損傷。
3. CST圓形strut提升支架與血管貼合度,側孔網眼提供最大程度擴張,易於複雜分叉病變病灶治療。
|
(一)於執行心導管氣球擴張術時(或術後二十四小時內)冠狀血管產生急性阻塞(ACUTE CLOSURE)或瀕臨急性阻塞狀況者(THREATENED CLOSURE),後者之診斷要件為需具有下列三個標準之一者: 1.內膜剝離長度大於十五毫米以上 2.對比劑在血管外顯影,嚴重度在Type B(含)以上 3.冠狀動脈病灶血流等級在TIMI2(含)或以下者。(二)原發性病灶(DE NOVO LESION)血管內徑大於等於2.5毫米,且經一比一之氣球與血管內徑比之氣球正常建議壓力擴張後,殘餘狹窄經測量仍大於百分之四十以上或殘餘狹窄經測量FFR≦0.8者。(三)經皮冠狀動脈擴張術後,原病灶再發狹窄大於百分之五十之病灶或再發狹窄經測量FFR≦0.8者。 (四)冠狀動脈繞道手術(CABG)後,繞道血管發生百分之七十以上之狹窄病灶。(五)特異病灶:1.開口處(ostial)病灶『參照【註】』及左主幹幹身病灶且血管內徑大於等於2.75毫米,狹窄大於等於70%或狹窄50-70%且FFR≦0.8者。2.慢性完全阻塞(二個月(含)以上)。
3.AMI 12小時(含)以內。4.經繞道手術後,繞道血管完全阻塞時,原冠狀動脈之介入性治療。
|
(一)同時設有心臟血管內科及心臟外科兩專科之特約醫院。(二)需為本局認可並經中華民國心臟學會認可之心臟專科醫師實施。
|
*Resolute Integrity支架禁止用於:
1. 對阿斯匹林、肝素、氯?格雷、?氯?定、mTOR抑制藥物如Zotarolimus (tacrolimus, sirolimus, everolimus)或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬或顯影劑有過敏症或過敏的患者。 2. 對抗血小板和/或抗血治療有禁忌症的病患。
3. 經診斷,患者的病變部位會阻礙血管成形球囊完全擴張,或者使支架或支架輸送系統無法正確放置。
*潛在的不良事件- 與冠狀動脈支架手術過程相關的不良事件或使用IVUS(血管內超音波設備)或PCI(經皮冠狀動脈介入)所引發的不良事件按嚴重程度列出如下:
‧ 死亡 ‧ 大量失血(需輸血急救)
‧ 動脈瘤、假性動脈瘤,或動靜脈廔管(AVF) ‧ 休克/肺水腫
‧ 支架變形、塌陷或破裂 ‧ 冠狀動脈痙攣
‧ 緊急手術:周邊或冠狀血管繞道手術 ‧ 突發血管閉鎖
‧ 中風/暫時缺血性發作(TIA) ‧ 低血壓/高血壓
‧ 心包填塞 ‧ 過敏反應(對顯影劑、抗血小板藥物,或支架系統- 金屬、藥物或聚合物塗層)
‧ 冠狀動脈堵塞、穿孔、破裂或剝離 ‧ 周邊缺血/周邊神經傷害
‧ 心包炎 ‧ 感染或發燒
‧ 栓塞(氣體、組織、裝置或血栓) ‧ 不穩定性心絞痛
‧ 血栓(急性、亞急性、慢性或極慢性) ‧ 入針部位疼痛、血腫或出血
‧ 支架貼壁不全 ‧ 球囊破裂
‧ 心肌梗塞(MI) ‧ 支架移位
‧ 安裝支架之動脈發生再狹窄 ‧ 支架安裝失敗
‧ 心律不整 ‧ 支架錯位
|
1. 使用專為塗藥支架設計之藥物塗層BioLinx,延長藥物釋放時間至180天,提供優越生物相容性並降低血管內皮細胞發炎反應所產生之支架血栓風險。 2. 提供Resolute全球臨床試驗計畫一年期數據顯示,植入Resolute塗藥支架「一個月後中斷或停止雙重抗血小板藥物治療(DAPT)之患者,其支架血栓形成率低」。儘管醫生應遵守目前 ESC或 ACC/ AHA/ SCAI經皮冠狀動脈介入治療準則,但患者於植入支架一個月或更長時間後中斷 DAPT藥物治療的風險被認為很低,且數據顯示不會增加支架血栓形成風險。Resolulte 全球臨床試驗計畫五年數據顯示支架血栓發生率僅1.2%。 3. 獲得美國FDA用於治療糖尿病患適應症之塗藥支架
|
| RONYX-450-12-X冠狀動脈塗藥支架(律動歐尼克斯) |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
Resolute Onyx支架由鈷合金及鉑銥合金構成,其上塗有基底塗層及藥物Zotarolimus與BioLinx聚合物系統的混合物。適用於適合接受經皮冠狀動脈成形術(PTCA)之病患。本支架為永久植入物。
|
Resolute Onyx支架系統適用於適合接受經皮冠狀動脈成形術之病患,其基準血管直徑介於2.0mm至4.0mm。Resolute Onyx支架適用於治療以下病患和病灶類型:
1.糖尿病
2.多支血管病變
3.急性冠狀動脈症候群(ACS)
4.急性心肌梗塞(AMI)
不穩定型心絞痛(UA)
|
禁止用於:
1.對阿司匹林(Aspirin), 肝素(Heparin), Clopidogrel, Ticlopidine, mTOR抑制藥物或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬、鉑和銥或顯影劑有過敏反應或過敏的病患。
2.對於抗血小板和/或抗凝血治療有禁忌症的病患。
|
1.下列副作用/併發症可能與 Zotarolimus的使用(但不限於)相關:貧血, 血尿, 口周感覺異常, 感染, 腹瀉, 疼痛(腹痛或關節痛), 皮膚乾燥, 皮疹, 頭痛
2. BioLinx聚合物的副作用/併發症與其他支架塗層相同,可能包括但不限於以下各項:支架植入部位出現局部性發炎,
植入支架的動脈再狹窄, 過敏反應
|
載有活性藥物Zotarolimus的Resolute Onyx支架用於降低在冠狀動脈介入治療中再狹窄化的發生。Resolute Onyx支架的標準藥物劑量為塗佈支架表面積1.6 μg/mm2 的Zotarolimus。
|
| RONYX-450-15-X冠狀動脈塗藥支架(律動歐尼克斯) |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
Resolute Onyx支架由鈷合金及鉑銥合金構成,其上塗有基底塗層及藥物Zotarolimus與BioLinx聚合物系統的混合物。適用於適合接受經皮冠狀動脈成形術(PTCA)之病患。本支架為永久植入物。
|
Resolute Onyx支架系統適用於適合接受經皮冠狀動脈成形術之病患,其基準血管直徑介於2.0mm至4.0mm。Resolute Onyx支架適用於治療以下病患和病灶類型:
1.糖尿病
2.多支血管病變
3.急性冠狀動脈症候群(ACS)
4.急性心肌梗塞(AMI)
不穩定型心絞痛(UA)
|
禁止用於:
1.對阿司匹林(Aspirin), 肝素(Heparin), Clopidogrel, Ticlopidine, mTOR抑制藥物或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬、鉑和銥或顯影劑有過敏反應或過敏的病患。
2.對於抗血小板和/或抗凝血治療有禁忌症的病患。
|
1.下列副作用/併發症可能與 Zotarolimus的使用(但不限於)相關:貧血, 血尿, 口周感覺異常, 感染, 腹瀉, 疼痛(腹痛或關節痛), 皮膚乾燥, 皮疹, 頭痛
2. BioLinx聚合物的副作用/併發症與其他支架塗層相同,可能包括但不限於以下各項:支架植入部位出現局部性發炎,
植入支架的動脈再狹窄, 過敏反應
|
載有活性藥物Zotarolimus的Resolute Onyx支架用於降低在冠狀動脈介入治療中再狹窄化的發生。Resolute Onyx支架的標準藥物劑量為塗佈支架表面積1.6 μg/mm2 的Zotarolimus。
|
| RONYX-450-15-X冠狀動脈塗藥支架(律動歐尼克斯) |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
Resolute Onyx支架由鈷合金及鉑銥合金構成,其上塗有基底塗層及藥物Zotarolimus與BioLinx聚合物系統的混合物。適用於適合接受經皮冠狀動脈成形術(PTCA)之病患。本支架為永久植入物。
|
Resolute Onyx支架系統適用於適合接受經皮冠狀動脈成形術之病患,其基準血管直徑介於2.0mm至4.0mm。Resolute Onyx支架適用於治療以下病患和病灶類型:
1.糖尿病
2.多支血管病變
3.急性冠狀動脈症候群(ACS)
4.急性心肌梗塞(AMI)
不穩定型心絞痛(UA)
|
禁止用於:
1.對阿司匹林(Aspirin), 肝素(Heparin), Clopidogrel, Ticlopidine, mTOR抑制藥物或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬、鉑和銥或顯影劑有過敏反應或過敏的病患。
2.對於抗血小板和/或抗凝血治療有禁忌症的病患。
|
1.下列副作用/併發症可能與 Zotarolimus的使用(但不限於)相關:貧血, 血尿, 口周感覺異常, 感染, 腹瀉, 疼痛(腹痛或關節痛), 皮膚乾燥, 皮疹, 頭痛
2. BioLinx聚合物的副作用/併發症與其他支架塗層相同,可能包括但不限於以下各項:支架植入部位出現局部性發炎,
植入支架的動脈再狹窄, 過敏反應
|
載有活性藥物Zotarolimus的Resolute Onyx支架用於降低在冠狀動脈介入治療中再狹窄化的發生。Resolute Onyx支架的標準藥物劑量為塗佈支架表面積1.6 μg/mm2 的Zotarolimus。
|
| RONYX-450-18-X冠狀動脈塗藥支架(律動歐尼克斯) |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
Resolute Onyx支架由鈷合金及鉑銥合金構成,其上塗有基底塗層及藥物Zotarolimus與BioLinx聚合物系統的混合物。適用於適合接受經皮冠狀動脈成形術(PTCA)之病患。本支架為永久植入物。
|
Resolute Onyx支架系統適用於適合接受經皮冠狀動脈成形術之病患,其基準血管直徑介於2.0mm至4.0mm。Resolute Onyx支架適用於治療以下病患和病灶類型:
1.糖尿病
2.多支血管病變
3.急性冠狀動脈症候群(ACS)
4.急性心肌梗塞(AMI)
不穩定型心絞痛(UA)
|
禁止用於:
1.對阿司匹林(Aspirin), 肝素(Heparin), Clopidogrel, Ticlopidine, mTOR抑制藥物或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬、鉑和銥或顯影劑有過敏反應或過敏的病患。
2.對於抗血小板和/或抗凝血治療有禁忌症的病患。
|
1.下列副作用/併發症可能與 Zotarolimus的使用(但不限於)相關:貧血, 血尿, 口周感覺異常, 感染, 腹瀉, 疼痛(腹痛或關節痛), 皮膚乾燥, 皮疹, 頭痛
2. BioLinx聚合物的副作用/併發症與其他支架塗層相同,可能包括但不限於以下各項:支架植入部位出現局部性發炎,
植入支架的動脈再狹窄, 過敏反應
|
載有活性藥物Zotarolimus的Resolute Onyx支架用於降低在冠狀動脈介入治療中再狹窄化的發生。Resolute Onyx支架的標準藥物劑量為塗佈支架表面積1.6 μg/mm2 的Zotarolimus。
|
| RONYX-450-18-X冠狀動脈塗藥支架(律動歐尼克斯) |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
Resolute Onyx支架由鈷合金及鉑銥合金構成,其上塗有基底塗層及藥物Zotarolimus與BioLinx聚合物系統的混合物。適用於適合接受經皮冠狀動脈成形術(PTCA)之病患。本支架為永久植入物。
|
Resolute Onyx支架系統適用於適合接受經皮冠狀動脈成形術之病患,其基準血管直徑介於2.0mm至4.0mm。Resolute Onyx支架適用於治療以下病患和病灶類型:
1.糖尿病
2.多支血管病變
3.急性冠狀動脈症候群(ACS)
4.急性心肌梗塞(AMI)
不穩定型心絞痛(UA)
|
禁止用於:
1.對阿司匹林(Aspirin), 肝素(Heparin), Clopidogrel, Ticlopidine, mTOR抑制藥物或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬、鉑和銥或顯影劑有過敏反應或過敏的病患。
2.對於抗血小板和/或抗凝血治療有禁忌症的病患。
|
1.下列副作用/併發症可能與 Zotarolimus的使用(但不限於)相關:貧血, 血尿, 口周感覺異常, 感染, 腹瀉, 疼痛(腹痛或關節痛), 皮膚乾燥, 皮疹, 頭痛
2. BioLinx聚合物的副作用/併發症與其他支架塗層相同,可能包括但不限於以下各項:支架植入部位出現局部性發炎,
植入支架的動脈再狹窄, 過敏反應
|
載有活性藥物Zotarolimus的Resolute Onyx支架用於降低在冠狀動脈介入治療中再狹窄化的發生。Resolute Onyx支架的標準藥物劑量為塗佈支架表面積1.6 μg/mm2 的Zotarolimus。
|
| RONYX-500-12-X冠狀動脈塗藥支架(律動歐尼克斯) |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
Resolute Onyx支架由鈷合金及鉑銥合金構成,其上塗有基底塗層及藥物Zotarolimus與BioLinx聚合物系統的混合物。適用於適合接受經皮冠狀動脈成形術(PTCA)之病患。本支架為永久植入物。
|
Resolute Onyx支架系統適用於適合接受經皮冠狀動脈成形術之病患,其基準血管直徑介於2.0mm至4.0mm。Resolute Onyx支架適用於治療以下病患和病灶類型:
1.糖尿病
2.多支血管病變
3.急性冠狀動脈症候群(ACS)
4.急性心肌梗塞(AMI)
不穩定型心絞痛(UA)
|
禁止用於:
1.對阿司匹林(Aspirin), 肝素(Heparin), Clopidogrel, Ticlopidine, mTOR抑制藥物或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬、鉑和銥或顯影劑有過敏反應或過敏的病患。
2.對於抗血小板和/或抗凝血治療有禁忌症的病患。
|
1.下列副作用/併發症可能與 Zotarolimus的使用(但不限於)相關:貧血, 血尿, 口周感覺異常, 感染, 腹瀉, 疼痛(腹痛或關節痛), 皮膚乾燥, 皮疹, 頭痛
2. BioLinx聚合物的副作用/併發症與其他支架塗層相同,可能包括但不限於以下各項:支架植入部位出現局部性發炎,
植入支架的動脈再狹窄, 過敏反應
|
載有活性藥物Zotarolimus的Resolute Onyx支架用於降低在冠狀動脈介入治療中再狹窄化的發生。Resolute Onyx支架的標準藥物劑量為塗佈支架表面積1.6 μg/mm2 的Zotarolimus。
|
| RONYX-500-12-X冠狀動脈塗藥支架(律動歐尼克斯) |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
Resolute Onyx支架由鈷合金及鉑銥合金構成,其上塗有基底塗層及藥物Zotarolimus與BioLinx聚合物系統的混合物。適用於適合接受經皮冠狀動脈成形術(PTCA)之病患。本支架為永久植入物。
|
Resolute Onyx支架系統適用於適合接受經皮冠狀動脈成形術之病患,其基準血管直徑介於2.0mm至4.0mm。Resolute Onyx支架適用於治療以下病患和病灶類型:
1.糖尿病
2.多支血管病變
3.急性冠狀動脈症候群(ACS)
4.急性心肌梗塞(AMI)
不穩定型心絞痛(UA)
|
禁止用於:
1.對阿司匹林(Aspirin), 肝素(Heparin), Clopidogrel, Ticlopidine, mTOR抑制藥物或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬、鉑和銥或顯影劑有過敏反應或過敏的病患。
2.對於抗血小板和/或抗凝血治療有禁忌症的病患。
|
1.下列副作用/併發症可能與 Zotarolimus的使用(但不限於)相關:貧血, 血尿, 口周感覺異常, 感染, 腹瀉, 疼痛(腹痛或關節痛), 皮膚乾燥, 皮疹, 頭痛
2. BioLinx聚合物的副作用/併發症與其他支架塗層相同,可能包括但不限於以下各項:支架植入部位出現局部性發炎,
植入支架的動脈再狹窄, 過敏反應
|
載有活性藥物Zotarolimus的Resolute Onyx支架用於降低在冠狀動脈介入治療中再狹窄化的發生。Resolute Onyx支架的標準藥物劑量為塗佈支架表面積1.6 μg/mm2 的Zotarolimus。
|
| RONYX-500-15-X冠狀動脈塗藥支架(律動歐尼克斯) |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
Resolute Onyx支架由鈷合金及鉑銥合金構成,其上塗有基底塗層及藥物Zotarolimus與BioLinx聚合物系統的混合物。適用於適合接受經皮冠狀動脈成形術(PTCA)之病患。本支架為永久植入物。
|
Resolute Onyx支架系統適用於適合接受經皮冠狀動脈成形術之病患,其基準血管直徑介於2.0mm至4.0mm。Resolute Onyx支架適用於治療以下病患和病灶類型:
1.糖尿病
2.多支血管病變
3.急性冠狀動脈症候群(ACS)
4.急性心肌梗塞(AMI)
不穩定型心絞痛(UA)
|
禁止用於:
1.對阿司匹林(Aspirin), 肝素(Heparin), Clopidogrel, Ticlopidine, mTOR抑制藥物或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬、鉑和銥或顯影劑有過敏反應或過敏的病患。
2.對於抗血小板和/或抗凝血治療有禁忌症的病患。
|
1.下列副作用/併發症可能與 Zotarolimus的使用(但不限於)相關:貧血, 血尿, 口周感覺異常, 感染, 腹瀉, 疼痛(腹痛或關節痛), 皮膚乾燥, 皮疹, 頭痛
2. BioLinx聚合物的副作用/併發症與其他支架塗層相同,可能包括但不限於以下各項:支架植入部位出現局部性發炎,
植入支架的動脈再狹窄, 過敏反應
|
載有活性藥物Zotarolimus的Resolute Onyx支架用於降低在冠狀動脈介入治療中再狹窄化的發生。Resolute Onyx支架的標準藥物劑量為塗佈支架表面積1.6 μg/mm2 的Zotarolimus。
|
| RONYX-500-15-X冠狀動脈塗藥支架(律動歐尼克斯) |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
Resolute Onyx支架由鈷合金及鉑銥合金構成,其上塗有基底塗層及藥物Zotarolimus與BioLinx聚合物系統的混合物。適用於適合接受經皮冠狀動脈成形術(PTCA)之病患。本支架為永久植入物。
|
Resolute Onyx支架系統適用於適合接受經皮冠狀動脈成形術之病患,其基準血管直徑介於2.0mm至4.0mm。Resolute Onyx支架適用於治療以下病患和病灶類型:
1.糖尿病
2.多支血管病變
3.急性冠狀動脈症候群(ACS)
4.急性心肌梗塞(AMI)
不穩定型心絞痛(UA)
|
禁止用於:
1.對阿司匹林(Aspirin), 肝素(Heparin), Clopidogrel, Ticlopidine, mTOR抑制藥物或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬、鉑和銥或顯影劑有過敏反應或過敏的病患。
2.對於抗血小板和/或抗凝血治療有禁忌症的病患。
|
1.下列副作用/併發症可能與 Zotarolimus的使用(但不限於)相關:貧血, 血尿, 口周感覺異常, 感染, 腹瀉, 疼痛(腹痛或關節痛), 皮膚乾燥, 皮疹, 頭痛
2. BioLinx聚合物的副作用/併發症與其他支架塗層相同,可能包括但不限於以下各項:支架植入部位出現局部性發炎,
植入支架的動脈再狹窄, 過敏反應
|
載有活性藥物Zotarolimus的Resolute Onyx支架用於降低在冠狀動脈介入治療中再狹窄化的發生。Resolute Onyx支架的標準藥物劑量為塗佈支架表面積1.6 μg/mm2 的Zotarolimus。
|
| RONYX-500-18-X冠狀動脈塗藥支架(律動歐尼克斯) |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
Resolute Onyx支架由鈷合金及鉑銥合金構成,其上塗有基底塗層及藥物Zotarolimus與BioLinx聚合物系統的混合物。適用於適合接受經皮冠狀動脈成形術(PTCA)之病患。本支架為永久植入物。
|
Resolute Onyx支架系統適用於適合接受經皮冠狀動脈成形術之病患,其基準血管直徑介於2.0mm至4.0mm。Resolute Onyx支架適用於治療以下病患和病灶類型:
1.糖尿病
2.多支血管病變
3.急性冠狀動脈症候群(ACS)
4.急性心肌梗塞(AMI)
不穩定型心絞痛(UA)
|
禁止用於:
1.對阿司匹林(Aspirin), 肝素(Heparin), Clopidogrel, Ticlopidine, mTOR抑制藥物或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬、鉑和銥或顯影劑有過敏反應或過敏的病患。
2.對於抗血小板和/或抗凝血治療有禁忌症的病患。
|
1.下列副作用/併發症可能與 Zotarolimus的使用(但不限於)相關:貧血, 血尿, 口周感覺異常, 感染, 腹瀉, 疼痛(腹痛或關節痛), 皮膚乾燥, 皮疹, 頭痛
2. BioLinx聚合物的副作用/併發症與其他支架塗層相同,可能包括但不限於以下各項:支架植入部位出現局部性發炎,
植入支架的動脈再狹窄, 過敏反應
|
載有活性藥物Zotarolimus的Resolute Onyx支架用於降低在冠狀動脈介入治療中再狹窄化的發生。Resolute Onyx支架的標準藥物劑量為塗佈支架表面積1.6 μg/mm2 的Zotarolimus。
|
| RONYX-500-18-X冠狀動脈塗藥支架(律動歐尼克斯) |  | MEDTRONIC | $73,412.00 | $14,099.00 | $59,313.00 | |
Resolute Onyx支架由鈷合金及鉑銥合金構成,其上塗有基底塗層及藥物Zotarolimus與BioLinx聚合物系統的混合物。適用於適合接受經皮冠狀動脈成形術(PTCA)之病患。本支架為永久植入物。
|
Resolute Onyx支架系統適用於適合接受經皮冠狀動脈成形術之病患,其基準血管直徑介於2.0mm至4.0mm。Resolute Onyx支架適用於治療以下病患和病灶類型:
1.糖尿病
2.多支血管病變
3.急性冠狀動脈症候群(ACS)
4.急性心肌梗塞(AMI)
不穩定型心絞痛(UA)
|
禁止用於:
1.對阿司匹林(Aspirin), 肝素(Heparin), Clopidogrel, Ticlopidine, mTOR抑制藥物或任何其他mTOR抑制劑類似物或衍生物、聚合物、鈷、鉻、鎳、鉬、鉑和銥或顯影劑有過敏反應或過敏的病患。
2.對於抗血小板和/或抗凝血治療有禁忌症的病患。
|
1.下列副作用/併發症可能與 Zotarolimus的使用(但不限於)相關:貧血, 血尿, 口周感覺異常, 感染, 腹瀉, 疼痛(腹痛或關節痛), 皮膚乾燥, 皮疹, 頭痛
2. BioLinx聚合物的副作用/併發症與其他支架塗層相同,可能包括但不限於以下各項:支架植入部位出現局部性發炎,
植入支架的動脈再狹窄, 過敏反應
|
載有活性藥物Zotarolimus的Resolute Onyx支架用於降低在冠狀動脈介入治療中再狹窄化的發生。Resolute Onyx支架的標準藥物劑量為塗佈支架表面積1.6 μg/mm2 的Zotarolimus。
|
| SBI05008013P紫杉醇塗藥周邊球囊導管(愛德米羅) |  | MEDTRONIC | $49,773.00 | $28,773.00 | $21,000.00 | |
本產品的球囊上塗有FreePac藥物塗層,含有紫杉醇及賦形劑尿素。球囊導管由經皮腔內血管成形術物理性擴張血管,而藥物塗層則用於降低導致再挾窄的增生反應。紫杉醇用於穩定微管以降低細胞增生。
|
本產品適用於患有周邊動脈阻塞性疾病(包含支架內再狹窄(ISR))及患友自體或人工動靜脈透析廔管阻塞性病灶患者經皮腔內血管成形術(PTA)。
|
在放入擴張導管前,應按照經皮腔內血管成形術的標準治療程序給于患者適當的藥物治療。為使空氣進入減至最少,請抽吸並沖洗系統,並於全程手術保持導管緊密連接。應於治療前確認病患是否會對於顯影劑、抗血小板治療、求囊導管和FreePac塗層有過敏反應…..等。
|
急性血管閉塞/血栓形成。進入部位疼痛、血腫、出血/和局部感染。對顯影劑、抗血小板治療或導管系統組件的過敏反應。心律不整。球囊破裂。死亡。動脈剝離、穿孔或破裂。心內膜炎。熱源反應。敗血症/感染………等。
|
健保品無藥物塗層,病灶處容易再狹窄、細胞增生。
|
| SBI05008013P紫杉醇塗藥周邊球囊導管(愛德米羅) |  | MEDTRONIC | $49,773.00 | $28,773.00 | $21,000.00 | |
本產品的球囊上塗有FreePac藥物塗層,含有紫杉醇及賦形劑尿素。球囊導管由經皮腔內血管成形術物理性擴張血管,而藥物塗層則用於降低導致再挾窄的增生反應。紫杉醇用於穩定微管以降低細胞增生。
|
本產品適用於患有周邊動脈阻塞性疾病(包含支架內再狹窄(ISR))及患友自體或人工動靜脈透析廔管阻塞性病灶患者經皮腔內血管成形術(PTA)。
|
在放入擴張導管前,應按照經皮腔內血管成形術的標準治療程序給于患者適當的藥物治療。為使空氣進入減至最少,請抽吸並沖洗系統,並於全程手術保持導管緊密連接。應於治療前確認病患是否會對於顯影劑、抗血小板治療、求囊導管和FreePac塗層有過敏反應…..等。
|
急性血管閉塞/血栓形成。進入部位疼痛、血腫、出血/和局部感染。對顯影劑、抗血小板治療或導管系統組件的過敏反應。心律不整。球囊破裂。死亡。動脈剝離、穿孔或破裂。心內膜炎。熱源反應。敗血症/感染………等。
|
健保品無藥物塗層,病灶處容易再狹窄、細胞增生。
|
| SBI05012013P紫杉醇塗藥周邊球囊導管(愛德米羅) |  | MEDTRONIC | $49,773.00 | $28,773.00 | $21,000.00 | |
本產品的球囊上塗有FreePac藥物塗層,含有紫杉醇及賦形劑尿素。球囊導管由經皮腔內血管成形術物理性擴張血管,而藥物塗層則用於降低導致再挾窄的增生反應。紫杉醇用於穩定微管以降低細胞增生。
|
本產品適用於患有周邊動脈阻塞性疾病(包含支架內再狹窄(ISR))及患友自體或人工動靜脈透析廔管阻塞性病灶患者經皮腔內血管成形術(PTA)。
|
在放入擴張導管前,應按照經皮腔內血管成形術的標準治療程序給于患者適當的藥物治療。為使空氣進入減至最少,請抽吸並沖洗系統,並於全程手術保持導管緊密連接。應於治療前確認病患是否會對於顯影劑、抗血小板治療、求囊導管和FreePac塗層有過敏反應…..等。
|
急性血管閉塞/血栓形成。進入部位疼痛、血腫、出血/和局部感染。對顯影劑、抗血小板治療或導管系統組件的過敏反應。心律不整。球囊破裂。死亡。動脈剝離、穿孔或破裂。心內膜炎。熱源反應。敗血症/感染………等。
|
健保品無藥物塗層,病灶處容易再狹窄、細胞增生。
|
| SBI05012013P紫杉醇塗藥周邊球囊導管(愛德米羅) |  | MEDTRONIC | $49,773.00 | $28,773.00 | $21,000.00 | |
本產品的球囊上塗有FreePac藥物塗層,含有紫杉醇及賦形劑尿素。球囊導管由經皮腔內血管成形術物理性擴張血管,而藥物塗層則用於降低導致再挾窄的增生反應。紫杉醇用於穩定微管以降低細胞增生。
|
本產品適用於患有周邊動脈阻塞性疾病(包含支架內再狹窄(ISR))及患友自體或人工動靜脈透析廔管阻塞性病灶患者經皮腔內血管成形術(PTA)。
|
在放入擴張導管前,應按照經皮腔內血管成形術的標準治療程序給于患者適當的藥物治療。為使空氣進入減至最少,請抽吸並沖洗系統,並於全程手術保持導管緊密連接。應於治療前確認病患是否會對於顯影劑、抗血小板治療、求囊導管和FreePac塗層有過敏反應…..等。
|
急性血管閉塞/血栓形成。進入部位疼痛、血腫、出血/和局部感染。對顯影劑、抗血小板治療或導管系統組件的過敏反應。心律不整。球囊破裂。死亡。動脈剝離、穿孔或破裂。心內膜炎。熱源反應。敗血症/感染………等。
|
健保品無藥物塗層,病灶處容易再狹窄、細胞增生。
|
| SBI05015013P紫杉醇塗藥周邊球囊導管(愛德米羅) |  | MEDTRONIC | $49,773.00 | $28,773.00 | $21,000.00 | |
本產品的球囊上塗有FreePac藥物塗層,含有紫杉醇及賦形劑尿素。球囊導管由經皮腔內血管成形術物理性擴張血管,而藥物塗層則用於降低導致再挾窄的增生反應。紫杉醇用於穩定微管以降低細胞增生。
|
本產品適用於患有周邊動脈阻塞性疾病(包含支架內再狹窄(ISR))及患友自體或人工動靜脈透析廔管阻塞性病灶患者經皮腔內血管成形術(PTA)。
|
在放入擴張導管前,應按照經皮腔內血管成形術的標準治療程序給于患者適當的藥物治療。為使空氣進入減至最少,請抽吸並沖洗系統,並於全程手術保持導管緊密連接。應於治療前確認病患是否會對於顯影劑、抗血小板治療、求囊導管和FreePac塗層有過敏反應…..等。
|
急性血管閉塞/血栓形成。進入部位疼痛、血腫、出血/和局部感染。對顯影劑、抗血小板治療或導管系統組件的過敏反應。心律不整。球囊破裂。死亡。動脈剝離、穿孔或破裂。心內膜炎。熱源反應。敗血症/感染………等。
|
健保品無藥物塗層,病灶處容易再狹窄、細胞增生。
|
| SBI05015013P紫杉醇塗藥周邊球囊導管(愛德米羅) |  | MEDTRONIC | $49,773.00 | $28,773.00 | $21,000.00 | |
本產品的球囊上塗有FreePac藥物塗層,含有紫杉醇及賦形劑尿素。球囊導管由經皮腔內血管成形術物理性擴張血管,而藥物塗層則用於降低導致再挾窄的增生反應。紫杉醇用於穩定微管以降低細胞增生。
|
本產品適用於患有周邊動脈阻塞性疾病(包含支架內再狹窄(ISR))及患友自體或人工動靜脈透析廔管阻塞性病灶患者經皮腔內血管成形術(PTA)。
|
在放入擴張導管前,應按照經皮腔內血管成形術的標準治療程序給于患者適當的藥物治療。為使空氣進入減至最少,請抽吸並沖洗系統,並於全程手術保持導管緊密連接。應於治療前確認病患是否會對於顯影劑、抗血小板治療、求囊導管和FreePac塗層有過敏反應…..等。
|
急性血管閉塞/血栓形成。進入部位疼痛、血腫、出血/和局部感染。對顯影劑、抗血小板治療或導管系統組件的過敏反應。心律不整。球囊破裂。死亡。動脈剝離、穿孔或破裂。心內膜炎。熱源反應。敗血症/感染………等。
|
健保品無藥物塗層,病灶處容易再狹窄、細胞增生。
|
| SBI06008013P紫杉醇塗藥周邊球囊導管(愛德米羅) |  | MEDTRONIC | $49,773.00 | $28,773.00 | $21,000.00 | |
本產品的球囊上塗有FreePac藥物塗層,含有紫杉醇及賦形劑尿素。球囊導管由經皮腔內血管成形術物理性擴張血管,而藥物塗層則用於降低導致再挾窄的增生反應。紫杉醇用於穩定微管以降低細胞增生。
|
本產品適用於患有周邊動脈阻塞性疾病(包含支架內再狹窄(ISR))及患友自體或人工動靜脈透析廔管阻塞性病灶患者經皮腔內血管成形術(PTA)。
|
在放入擴張導管前,應按照經皮腔內血管成形術的標準治療程序給于患者適當的藥物治療。為使空氣進入減至最少,請抽吸並沖洗系統,並於全程手術保持導管緊密連接。應於治療前確認病患是否會對於顯影劑、抗血小板治療、求囊導管和FreePac塗層有過敏反應…..等。
|
急性血管閉塞/血栓形成。進入部位疼痛、血腫、出血/和局部感染。對顯影劑、抗血小板治療或導管系統組件的過敏反應。心律不整。球囊破裂。死亡。動脈剝離、穿孔或破裂。心內膜炎。熱源反應。敗血症/感染………等。
|
健保品無藥物塗層,病灶處容易再狹窄、細胞增生。
|
| SBI06008013P紫杉醇塗藥周邊球囊導管(愛德米羅) |  | MEDTRONIC | $49,773.00 | $28,773.00 | $21,000.00 | |
本產品的球囊上塗有FreePac藥物塗層,含有紫杉醇及賦形劑尿素。球囊導管由經皮腔內血管成形術物理性擴張血管,而藥物塗層則用於降低導致再挾窄的增生反應。紫杉醇用於穩定微管以降低細胞增生。
|
本產品適用於患有周邊動脈阻塞性疾病(包含支架內再狹窄(ISR))及患友自體或人工動靜脈透析廔管阻塞性病灶患者經皮腔內血管成形術(PTA)。
|
在放入擴張導管前,應按照經皮腔內血管成形術的標準治療程序給于患者適當的藥物治療。為使空氣進入減至最少,請抽吸並沖洗系統,並於全程手術保持導管緊密連接。應於治療前確認病患是否會對於顯影劑、抗血小板治療、求囊導管和FreePac塗層有過敏反應…..等。
|
急性血管閉塞/血栓形成。進入部位疼痛、血腫、出血/和局部感染。對顯影劑、抗血小板治療或導管系統組件的過敏反應。心律不整。球囊破裂。死亡。動脈剝離、穿孔或破裂。心內膜炎。熱源反應。敗血症/感染………等。
|
健保品無藥物塗層,病灶處容易再狹窄、細胞增生。
|
| SBI06012013P紫杉醇塗藥周邊球囊導管(愛德米羅) |  | MEDTRONIC | $49,773.00 | $28,773.00 | $21,000.00 | |
本產品的球囊上塗有FreePac藥物塗層,含有紫杉醇及賦形劑尿素。球囊導管由經皮腔內血管成形術物理性擴張血管,而藥物塗層則用於降低導致再挾窄的增生反應。紫杉醇用於穩定微管以降低細胞增生。
|
本產品適用於患有周邊動脈阻塞性疾病(包含支架內再狹窄(ISR))及患友自體或人工動靜脈透析廔管阻塞性病灶患者經皮腔內血管成形術(PTA)。
|
在放入擴張導管前,應按照經皮腔內血管成形術的標準治療程序給于患者適當的藥物治療。為使空氣進入減至最少,請抽吸並沖洗系統,並於全程手術保持導管緊密連接。應於治療前確認病患是否會對於顯影劑、抗血小板治療、求囊導管和FreePac塗層有過敏反應…..等。
|
急性血管閉塞/血栓形成。進入部位疼痛、血腫、出血/和局部感染。對顯影劑、抗血小板治療或導管系統組件的過敏反應。心律不整。球囊破裂。死亡。動脈剝離、穿孔或破裂。心內膜炎。熱源反應。敗血症/感染………等。
|
健保品無藥物塗層,病灶處容易再狹窄、細胞增生。
|
| SBI06012013P紫杉醇塗藥周邊球囊導管(愛德米羅) |  | MEDTRONIC | $49,773.00 | $28,773.00 | $21,000.00 | |
本產品的球囊上塗有FreePac藥物塗層,含有紫杉醇及賦形劑尿素。球囊導管由經皮腔內血管成形術物理性擴張血管,而藥物塗層則用於降低導致再挾窄的增生反應。紫杉醇用於穩定微管以降低細胞增生。
|
本產品適用於患有周邊動脈阻塞性疾病(包含支架內再狹窄(ISR))及患友自體或人工動靜脈透析廔管阻塞性病灶患者經皮腔內血管成形術(PTA)。
|
在放入擴張導管前,應按照經皮腔內血管成形術的標準治療程序給于患者適當的藥物治療。為使空氣進入減至最少,請抽吸並沖洗系統,並於全程手術保持導管緊密連接。應於治療前確認病患是否會對於顯影劑、抗血小板治療、求囊導管和FreePac塗層有過敏反應…..等。
|
急性血管閉塞/血栓形成。進入部位疼痛、血腫、出血/和局部感染。對顯影劑、抗血小板治療或導管系統組件的過敏反應。心律不整。球囊破裂。死亡。動脈剝離、穿孔或破裂。心內膜炎。熱源反應。敗血症/感染………等。
|
健保品無藥物塗層,病灶處容易再狹窄、細胞增生。
|
| SBI06015013P紫杉醇塗藥周邊球囊導管(愛德米羅) |  | MEDTRONIC | $49,773.00 | $28,773.00 | $21,000.00 | |
本產品的球囊上塗有FreePac藥物塗層,含有紫杉醇及賦形劑尿素。球囊導管由經皮腔內血管成形術物理性擴張血管,而藥物塗層則用於降低導致再挾窄的增生反應。紫杉醇用於穩定微管以降低細胞增生。
|
本產品適用於患有周邊動脈阻塞性疾病(包含支架內再狹窄(ISR))及患友自體或人工動靜脈透析廔管阻塞性病灶患者經皮腔內血管成形術(PTA)。
|
在放入擴張導管前,應按照經皮腔內血管成形術的標準治療程序給于患者適當的藥物治療。為使空氣進入減至最少,請抽吸並沖洗系統,並於全程手術保持導管緊密連接。應於治療前確認病患是否會對於顯影劑、抗血小板治療、求囊導管和FreePac塗層有過敏反應…..等。
|
急性血管閉塞/血栓形成。進入部位疼痛、血腫、出血/和局部感染。對顯影劑、抗血小板治療或導管系統組件的過敏反應。心律不整。球囊破裂。死亡。動脈剝離、穿孔或破裂。心內膜炎。熱源反應。敗血症/感染………等。
|
健保品無藥物塗層,病灶處容易再狹窄、細胞增生。
|
| SBI06015013P紫杉醇塗藥周邊球囊導管(愛德米羅) |  | MEDTRONIC | $49,773.00 | $28,773.00 | $21,000.00 | |
本產品的球囊上塗有FreePac藥物塗層,含有紫杉醇及賦形劑尿素。球囊導管由經皮腔內血管成形術物理性擴張血管,而藥物塗層則用於降低導致再挾窄的增生反應。紫杉醇用於穩定微管以降低細胞增生。
|
本產品適用於患有周邊動脈阻塞性疾病(包含支架內再狹窄(ISR))及患友自體或人工動靜脈透析廔管阻塞性病灶患者經皮腔內血管成形術(PTA)。
|
在放入擴張導管前,應按照經皮腔內血管成形術的標準治療程序給于患者適當的藥物治療。為使空氣進入減至最少,請抽吸並沖洗系統,並於全程手術保持導管緊密連接。應於治療前確認病患是否會對於顯影劑、抗血小板治療、求囊導管和FreePac塗層有過敏反應…..等。
|
急性血管閉塞/血栓形成。進入部位疼痛、血腫、出血/和局部感染。對顯影劑、抗血小板治療或導管系統組件的過敏反應。心律不整。球囊破裂。死亡。動脈剝離、穿孔或破裂。心內膜炎。熱源反應。敗血症/感染………等。
|
健保品無藥物塗層,病灶處容易再狹窄、細胞增生。
|
| SBI07008013P紫杉醇塗藥周邊球囊導管(愛德米羅) |  | MEDTRONIC | $49,773.00 | $28,773.00 | $21,000.00 | |
本產品的球囊上塗有FreePac藥物塗層,含有紫杉醇及賦形劑尿素。球囊導管由經皮腔內血管成形術物理性擴張血管,而藥物塗層則用於降低導致再挾窄的增生反應。紫杉醇用於穩定微管以降低細胞增生。
|
本產品適用於患有周邊動脈阻塞性疾病(包含支架內再狹窄(ISR))及患友自體或人工動靜脈透析廔管阻塞性病灶患者經皮腔內血管成形術(PTA)。
|
在放入擴張導管前,應按照經皮腔內血管成形術的標準治療程序給于患者適當的藥物治療。為使空氣進入減至最少,請抽吸並沖洗系統,並於全程手術保持導管緊密連接。應於治療前確認病患是否會對於顯影劑、抗血小板治療、求囊導管和FreePac塗層有過敏反應…..等。
|
急性血管閉塞/血栓形成。進入部位疼痛、血腫、出血/和局部感染。對顯影劑、抗血小板治療或導管系統組件的過敏反應。心律不整。球囊破裂。死亡。動脈剝離、穿孔或破裂。心內膜炎。熱源反應。敗血症/感染………等。
|
健保品無藥物塗層,病灶處容易再狹窄、細胞增生。
|
| SBI07008013P紫杉醇塗藥周邊球囊導管(愛德米羅) |  | MEDTRONIC | $49,773.00 | $28,773.00 | $21,000.00 | |
本產品的球囊上塗有FreePac藥物塗層,含有紫杉醇及賦形劑尿素。球囊導管由經皮腔內血管成形術物理性擴張血管,而藥物塗層則用於降低導致再挾窄的增生反應。紫杉醇用於穩定微管以降低細胞增生。
|
本產品適用於患有周邊動脈阻塞性疾病(包含支架內再狹窄(ISR))及患友自體或人工動靜脈透析廔管阻塞性病灶患者經皮腔內血管成形術(PTA)。
|
在放入擴張導管前,應按照經皮腔內血管成形術的標準治療程序給于患者適當的藥物治療。為使空氣進入減至最少,請抽吸並沖洗系統,並於全程手術保持導管緊密連接。應於治療前確認病患是否會對於顯影劑、抗血小板治療、求囊導管和FreePac塗層有過敏反應…..等。
|
急性血管閉塞/血栓形成。進入部位疼痛、血腫、出血/和局部感染。對顯影劑、抗血小板治療或導管系統組件的過敏反應。心律不整。球囊破裂。死亡。動脈剝離、穿孔或破裂。心內膜炎。熱源反應。敗血症/感染………等。
|
健保品無藥物塗層,病灶處容易再狹窄、細胞增生。
|
| 2.8MM高強度縫線固定釘(阿碩柯爾 縫合錨釘) |  | 阿碩柯爾 | $25,290.00 | $10,116.00 | $15,174.00 | |
1.2.8 mm All suture anchor 帶兩條二號MagnumWire縫線,強度佳 2.減少異物感 ,球狀植入物設計平均pull out受力面積 3.依照病人Bone quality去擴大 增強固定效果
|
適用於連接軟組織於肩、足、踝、肘、膝、手、腕與髖骨頭上之固定,固定於Rotator cuff tear repair 用純縫線固定方式,因無植入物,可降低異物感
|
單一次性使用
|
無
|
健保品項帶線錨釘為金屬材質,患者痊癒之後,金屬錨釘會留在骨頭裡,少數患者會感到異物感
|
| 5.5mm高強度寬帶中空可吸收錨釘(72203708) |  | 史耐輝 | $32,187.00 | $12,874.00 | $19,313.00 | |
1.全新螺紋設計,鎖入Bone裡更強的 Pullout力度達35ibf
2.錨釘唯一使用Ultratape縫線,提供更寬更多的接觸面積
3.加入硫酸鈣成份比起PLLA-HA讓病人術後骨質吸收更快更完整
|
適用於連接軟組織於肩及膝關節骨頭上之固定
|
單一次性使用
|
無
|
健保品項帶線錨釘為金屬材質,患者痊癒之後,金屬錨釘會留在骨頭裡,少數患者會感到異物感
|
| 5.5mm高強度中空骨活性免綁線錨釘(72205135) | 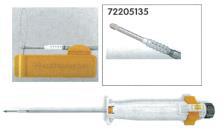 | 史耐輝 | $32,187.00 | $12,874.00 | $19,313.00 | |
1. Regenesorb材質配方,文獻證實21個月植入物80%被人體吸收;24個月近80%
長出骨組織。
2. 中空設計,植入後讓骨髓更易流出,文獻證實術後6周,病患旋轉肌韌帶復原
生長較厚。
3. 內部固定與介面固定設計,增加植入物固定力,與固定縫線的能力。
4. 改良穿線裝置,與大孔洞設計,醫師手術穿線更加容易,節省手術時間。
|
適用於連接軟組織於肩及膝關節骨頭上之固定
|
單一次性使用
|
無
|
健保品項帶線錨釘為金屬材質,患者痊癒之後,金屬錨釘會留在骨頭裡,少數患者會感到異物感
|
| 微型免綁線縫合錨釘(72205020) | 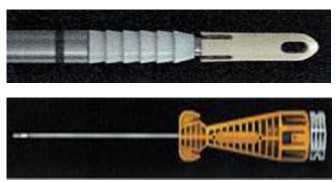 | 史耐輝 | $32,187.00 | $12,874.00 | $19,313.00 | |
本產品為一種固定裝置,目的在於將軟組織牢固的連結回骨頭。本產品含有已裝置插入器之縫合錨釘。為滅菌包裝,限單次使之產品。
|
本產品適用於重新連接下列適應症之軟組織與骨頭:
髖關節:
髖關節囊膜之修補與重建
肩寬節:
關節囊膜的穩定
- 班卡氏修補
- 前肩膀不穩定
- 前上肩關節唇損傷修補
- 關節囊膜之位移或是囊膜唇緣之重建
肱二頭肌腱固定術
|
限單次使用產品。
|
無
|
健保品項帶線錨釘為金屬材質,患者痊癒之後,金屬錨釘會留在骨頭裡,少數患者會感到異物感
|
| 免綁線縫合錨釘3.5-5.5mm(思維拉克中空縫合錨釘) |  | ARTHREX | $32,187.00 | $12,874.00 | $19,313.00 | |
1.可對抗關節分離亦可提早活動
2.不須二次手術移除
3.無斷裂可能,固定效果比傳統螺絲佳
4.除骨頭固定外,可代替韌帶與組織在癒合過程的固定
|
本產品是用於將組織固定縫合至骨頭上的固定物,適用於腳、踝、膝、手、腕、肘、肩、髖,如肩旋轉袖斷裂修復與韌帶重建等,普遍使用於外科手術中將軟組織固定縫合至骨頭上
|
1.單次使用,不可重複滅菌使用
2.手術後至完全癒合前,患處都需被保護
|
1.可能會有深層或表面的感染
2.對植入的材料過敏或有其他的反應
|
此產品是由聚孔酸Poly(L-Lactide)和/或polyetheretherketone (PEEK) 組成。並使用高鋼性縫合線提供更穩定的縫合效果,降低線材斷裂的發生機率。
|
| 4.75MM高鋼性加壓免綁線螺紋錨釘AR-2324BCCT |  | 艾思瑞斯 | $32,187.00 | $12,874.00 | $19,313.00 | |
1.錨釘完全中空及外側孔洞設計,可使骨髓液流入錨釘內,加速骨癒合生長。
2.加壓式免綁線設計,固定效果好亦能減少手術時間。
3.錨釘前端eyelet帶線孔洞設計,可調整修復後的韌帶鬆緊度後再將螺絲鎖入。
4.尾端縫線設計,可再做額外的修補更加強固定效果。
5.縫合線材為編織型寬版帶狀縫線,可避免軟組織受力後被線材切割
|
本產品是用於將組織固定縫合至骨頭上的固定物,適用於腳、踝、膝、手、腕、肘、肩、髖,如肩旋轉袖斷裂修復與韌帶重建等,普遍使用於外科手術中將軟組織固定縫合至骨頭上
|
1.單次使用,不可重複滅菌使用
2.手術後至完全癒合前,患處都需被保護
|
1.可能會有深層或表面的感染
2.對植入的材料過敏或有其他的反應
|
縫線為寬型編織,軟組織受力後不易造成縫線切割現象,患者可提早進行復健,以達成更良好的癒後
|
| 4.75MM高剛性縫合帶縫合錨釘AR-2324BCCTT(思維拉克) |  | 艾思瑞斯 | $32,187.00 | $12,874.00 | $19,313.00 | |
使用SwiveLock Suture進行全關節鏡下suprapectora方法,除了具有穩固與安全的優點之外,還可避免接觸肱二頭肌肌腱上方的軟組織,使其維持良好的血液與神經供應,避免機械性刺激。且具有較高的破壞負載能力。
|
臨床研究中,使用Bio-SwiveLock suture-Anchor單肢肌腱固定法(single-limb tendon fixation)固定肱二頭肌肌腱長頭,相較於Biceptor tenodesis screw雙肢肌腱固定法(double-limb tendon fixation),具有較好的固定效果,可避免雙肢肌腱固定法造成的遠端V形分裂。使用SwiveLock Suture進行全關節鏡下suprapectora方法,除了具有穩固與安全的優點之外,還可避免接觸肱二頭肌肌腱上方的軟組織,使其維持良好的血液與神經供應,避免機械性刺激。且具有較高的破壞負載能力,穩定性較高,能減少醫源性損傷的機率。
|
手術後至完全癒合前,植入物都需要被保護。術後患者需依醫囑或復健師指示避免對植入物造成過大壓力。
|
深層或表面的感染、異物反應、PLA材質已有報告過敏反應。發生此反應有時必須取出植入物。再次植入前須考慮患者對產品材質的敏感程度。
|
在力學測試上發現傳統型的錨釘,連接線與錨釘間發生斷裂因而導致脫落或是手術失敗。使用健保給付縫合錨釘其縫合後所殘留的線結可能會引起磨耗與組織反應問題。在縫合鉚釘附上高剛性縫合帶,對於剛拉應力以及伸展的肌腱韌帶部位固定更強韌。
|
| 4.75X19.1 MM高剛性縫合帶縫合錨釘AR-2324PCT(肩) |  | 艾思瑞斯 | $32,187.00 | $12,874.00 | $19,313.00 | |
使用SwiveLock Suture進行全關節鏡下suprapectora方法,除了具有穩固與安全的優點之外,還可避免接觸肱二頭肌肌腱上方的軟組織,使其維持良好的血液與神經供應,避免機械性刺激。且具有較高的破壞負載能力。
|
臨床研究中,使用Bio-SwiveLock suture-Anchor單肢肌腱固定法(single-limb tendon fixation)固定肱二頭肌肌腱長頭,相較於Biceptor tenodesis screw雙肢肌腱固定法(double-limb tendon fixation),具有較好的固定效果,可避免雙肢肌腱固定法造成的遠端V形分裂。使用SwiveLock Suture進行全關節鏡下suprapectora方法,除了具有穩固與安全的優點之外,還可避免接觸肱二頭肌肌腱上方的軟組織,使其維持良好的血液與神經供應,避免機械性刺激。且具有較高的破壞負載能力,穩定性較高,能減少醫源性損傷的機率。
|
手術後至完全癒合前,植入物都需要被保護。術後患者需依醫囑或復健師指示避免對植入物造成過大壓力。
|
深層或表面的感染、異物反應、PLA材質已有報告過敏反應。發生此反應有時必須取出植入物。再次植入前須考慮患者對產品材質的敏感程度。
|
在力學測試上發現傳統型的錨釘,連接線與錨釘間發生斷裂因而導致脫落或是手術失敗。使用健保給付縫合錨釘其縫合後所殘留的線結可能會引起磨耗與組織反應問題。在縫合鉚釘附上高剛性縫合帶,對於剛拉應力以及伸展的肌腱韌帶部位固定更強韌。
|
| 4.75X19.1 MM高剛性縫合帶縫合錨釘AR-2324PCTT(肩) |  | 艾思瑞斯 | $32,187.00 | $12,874.00 | $19,313.00 | |
使用SwiveLock Suture進行全關節鏡下suprapectora方法,除了具有穩固與安全的優點之外,還可避免接觸肱二頭肌肌腱上方的軟組織,使其維持良好的血液與神經供應,避免機械性刺激。且具有較高的破壞負載能力。
|
臨床研究中,使用Bio-SwiveLock suture-Anchor單肢肌腱固定法(single-limb tendon fixation)固定肱二頭肌肌腱長頭,相較於Biceptor tenodesis screw雙肢肌腱固定法(double-limb tendon fixation),具有較好的固定效果,可避免雙肢肌腱固定法造成的遠端V形分裂。使用SwiveLock Suture進行全關節鏡下suprapectora方法,除了具有穩固與安全的優點之外,還可避免接觸肱二頭肌肌腱上方的軟組織,使其維持良好的血液與神經供應,避免機械性刺激。且具有較高的破壞負載能力,穩定性較高,能減少醫源性損傷的機率。
|
手術後至完全癒合前,植入物都需要被保護。術後患者需依醫囑或復健師指示避免對植入物造成過大壓力。
|
深層或表面的感染、異物反應、PLA材質已有報告過敏反應。發生此反應有時必須取出植入物。再次植入前須考慮患者對產品材質的敏感程度。
|
在力學測試上發現傳統型的錨釘,連接線與錨釘間發生斷裂因而導致脫落或是手術失敗。使用健保給付縫合錨釘其縫合後所殘留的線結可能會引起磨耗與組織反應問題。在縫合鉚釘附上高剛性縫合帶,對於剛拉應力以及伸展的肌腱韌帶部位固定更強韌。
|
| 3.5X15.8 MM高剛性縫合帶縫合錨釘AR-2325BCC(肩) |  | 艾思瑞斯 | $32,187.00 | $12,874.00 | $19,313.00 | |
使用SwiveLock Suture進行全關節鏡下suprapectora方法,除了具有穩固與安全的優點之外,還可避免接觸肱二頭肌肌腱上方的軟組織,使其維持良好的血液與神經供應,避免機械性刺激。且具有較高的破壞負載能力。
|
臨床研究中,使用Bio-SwiveLock suture-Anchor單肢肌腱固定法(single-limb tendon fixation)固定肱二頭肌肌腱長頭,相較於Biceptor tenodesis screw雙肢肌腱固定法(double-limb tendon fixation),具有較好的固定效果,可避免雙肢肌腱固定法造成的遠端V形分裂。使用SwiveLock Suture進行全關節鏡下suprapectora方法,除了具有穩固與安全的優點之外,還可避免接觸肱二頭肌肌腱上方的軟組織,使其維持良好的血液與神經供應,避免機械性刺激。且具有較高的破壞負載能力,穩定性較高,能減少醫源性損傷的機率。
|
手術後至完全癒合前,植入物都需要被保護。術後患者需依醫囑或復健師指示避免對植入物造成過大壓力。
|
深層或表面的感染、異物反應、PLA材質已有報告過敏反應。發生此反應有時必須取出植入物。再次植入前須考慮患者對產品材質的敏感程度。
|
在力學測試上發現傳統型的錨釘,連接線與錨釘間發生斷裂因而導致脫落或是手術失敗。使用健保給付縫合錨釘其縫合後所殘留的線結可能會引起磨耗與組織反應問題。在縫合鉚釘附上高剛性縫合帶,對於剛拉應力以及伸展的肌腱韌帶部位固定更強韌。
|
| 5.5X24.5 MM高剛性縫合帶縫合錨釘AR-2323SLM(肩) |  | 艾思瑞斯 | $32,187.00 | $12,874.00 | $19,313.00 | |
使用SwiveLock Suture進行全關節鏡下suprapectora方法,除了具有穩固與安全的優點之外,還可避免接觸肱二頭肌肌腱上方的軟組織,使其維持良好的血液與神經供應,避免機械性刺激。且具有較高的破壞負載能力。
|
臨床研究中,使用Bio-SwiveLock suture-Anchor單肢肌腱固定法(single-limb tendon fixation)固定肱二頭肌肌腱長頭,相較於Biceptor tenodesis screw雙肢肌腱固定法(double-limb tendon fixation),具有較好的固定效果,可避免雙肢肌腱固定法造成的遠端V形分裂。使用SwiveLock Suture進行全關節鏡下suprapectora方法,除了具有穩固與安全的優點之外,還可避免接觸肱二頭肌肌腱上方的軟組織,使其維持良好的血液與神經供應,避免機械性刺激。且具有較高的破壞負載能力,穩定性較高,能減少醫源性損傷的機率。
|
手術後至完全癒合前,植入物都需要被保護。術後患者需依醫囑或復健師指示避免對植入物造成過大壓力。
|
深層或表面的感染、異物反應、PLA材質已有報告過敏反應。發生此反應有時必須取出植入物。再次植入前須考慮患者對產品材質的敏感程度。
|
在力學測試上發現傳統型的錨釘,連接線與錨釘間發生斷裂因而導致脫落或是手術失敗。使用健保給付縫合錨釘其縫合後所殘留的線結可能會引起磨耗與組織反應問題。在縫合鉚釘附上高剛性縫合帶,對於剛拉應力以及伸展的肌腱韌帶部位固定更強韌。
|
| 3.5X8.5 MM高剛性縫合帶縫合錨釘AR-8978P(手腳踝) |  | 艾思瑞斯 | $32,187.00 | $12,874.00 | $19,313.00 | |
使用SwiveLock Suture進行全關節鏡下suprapectora方法,除了具有穩固與安全的優點之外,還可避免接觸肱二頭肌肌腱上方的軟組織,使其維持良好的血液與神經供應,避免機械性刺激。且具有較高的破壞負載能力。
|
臨床研究中,使用Bio-SwiveLock suture-Anchor單肢肌腱固定法(single-limb tendon fixation)固定肱二頭肌肌腱長頭,相較於Biceptor tenodesis screw雙肢肌腱固定法(double-limb tendon fixation),具有較好的固定效果,可避免雙肢肌腱固定法造成的遠端V形分裂。使用SwiveLock Suture進行全關節鏡下suprapectora方法,除了具有穩固與安全的優點之外,還可避免接觸肱二頭肌肌腱上方的軟組織,使其維持良好的血液與神經供應,避免機械性刺激。且具有較高的破壞負載能力,穩定性較高,能減少醫源性損傷的機率。
|
手術後至完全癒合前,植入物都需要被保護。術後患者需依醫囑或復健師指示避免對植入物造成過大壓力。
|
深層或表面的感染、異物反應、PLA材質已有報告過敏反應。發生此反應有時必須取出植入物。再次植入前須考慮患者對產品材質的敏感程度。
|
在力學測試上發現傳統型的錨釘,連接線與錨釘間發生斷裂因而導致脫落或是手術失敗。使用健保給付縫合錨釘其縫合後所殘留的線結可能會引起磨耗與組織反應問題。在縫合鉚釘附上高剛性縫合帶,對於剛拉應力以及伸展的肌腱韌帶部位固定更強韌。
|
| 3.5X13.5 MM高剛性縫合帶縫合錨釘AR-8979P(手腳踝) |  | 艾思瑞斯 | $32,187.00 | $12,874.00 | $19,313.00 | |
使用SwiveLock Suture進行全關節鏡下suprapectora方法,除了具有穩固與安全的優點之外,還可避免接觸肱二頭肌肌腱上方的軟組織,使其維持良好的血液與神經供應,避免機械性刺激。且具有較高的破壞負載能力。
|
臨床研究中,使用Bio-SwiveLock suture-Anchor單肢肌腱固定法(single-limb tendon fixation)固定肱二頭肌肌腱長頭,相較於Biceptor tenodesis screw雙肢肌腱固定法(double-limb tendon fixation),具有較好的固定效果,可避免雙肢肌腱固定法造成的遠端V形分裂。使用SwiveLock Suture進行全關節鏡下suprapectora方法,除了具有穩固與安全的優點之外,還可避免接觸肱二頭肌肌腱上方的軟組織,使其維持良好的血液與神經供應,避免機械性刺激。且具有較高的破壞負載能力,穩定性較高,能減少醫源性損傷的機率。
|
手術後至完全癒合前,植入物都需要被保護。術後患者需依醫囑或復健師指示避免對植入物造成過大壓力。
|
深層或表面的感染、異物反應、PLA材質已有報告過敏反應。發生此反應有時必須取出植入物。再次植入前須考慮患者對產品材質的敏感程度。
|
在力學測試上發現傳統型的錨釘,連接線與錨釘間發生斷裂因而導致脫落或是手術失敗。使用健保給付縫合錨釘其縫合後所殘留的線結可能會引起磨耗與組織反應問題。在縫合鉚釘附上高剛性縫合帶,對於剛拉應力以及伸展的肌腱韌帶部位固定更強韌。
|
| 1.4MM史賽克艾康尼斯縫合錨釘 3910-500-512 |  | STRYKER | $25,290.00 | $10,116.00 | $15,174.00 | |
錨釘固定力相較其他錨釘來得更強,但體積卻只有其他的1/2(1.4mm & 2.3mm),且能在有限的空間內植入錨釘對骨頭破壞性較小。
|
適用於肩、足、踝、膝、髖和肘部骨骼中的受損軟組織,透過縫合重新附著到骨頭上。
|
1.本產品是暫時性的體內固定設備,僅限單次使用。請丟棄任何打開或未使用的產品。
2.在準備固定部位時,對骨骼皮質層的過度移除可能會導致錨釘被拉出。
3.本產品必須在插入後再展開,以便史錨定壓向骨皮質。在插入後,如果錨釘張力不當,可能導致縫線鬆弛或錨釘拉出。
4.切勿向錨釘施加過度拉力或超過錨釘負荷,以免拉出設備或扯斷縫線。
5.應嚴格遵守醫生制定的手術後康復計畫以防止植入物不良反應的產生。
|
1.病人可能出現深度或淺度感染。
2.病人可能對裝置材料過敏或產生其他不適反應。
3.手術期間可能出現固定失敗或錨釘拉出。
|
錨釘固定力相較其他錨釘來得更強,但體積卻只有其他的1/2(1.4mm & 2.3mm),且能在有限的空間內植入錨釘對骨頭破壞性較小。
|
| 2.3MM史賽克艾康尼斯縫合錨釘 3910-500-522 |  | STRYKER | $25,290.00 | $10,116.00 | $15,174.00 | |
錨釘固定力相較其他錨釘來得更強,但體積卻只有其他的1/2(1.4mm & 2.3mm),且能在有限的空間內植入錨釘對骨頭破壞性較小。
|
適用於肩、足、踝、膝、髖和肘部骨骼中的受損軟組織,透過縫合重新附著到骨頭上。
|
1.本產品是暫時性的體內固定設備,僅限單次使用。請丟棄任何打開或未使用的產品。
2.在準備固定部位時,對骨骼皮質層的過度移除可能會導致錨釘被拉出。
3.本產品必須在插入後再展開,以便史錨定壓向骨皮質。在插入後,如果錨釘張力不當,可能導致縫線鬆弛或錨釘拉出。
4.切勿向錨釘施加過度拉力或超過錨釘負荷,以免拉出設備或扯斷縫線。
5.應嚴格遵守醫生制定的手術後康復計畫以防止植入物不良反應的產生。
|
1.病人可能出現深度或淺度感染。
2.病人可能對裝置材料過敏或產生其他不適反應。
3.手術期間可能出現固定失敗或錨釘拉出。
|
錨釘固定力相較其他錨釘來得更強,但體積卻只有其他的1/2(1.4mm & 2.3mm),且能在有限的空間內植入錨釘對骨頭破壞性較小。
|
| 寶楠耐籠三維多孔鈦合金椎間融合器(TLIF大顆) |  | 寶楠 | $118,096.00 | $23,619.00 | $94,477.00 | |
‧光滑輪廓圍繞粗糙表面,避免微創植入損傷軟組織 .頭端為拋光彈頭型設計,有利於撐開進入椎間位置,也方便術中調整植入物方向 ‧尾端具備抗衝擊結構,可承受植入過程的敲擊 ‧連通多孔結構,適合骨細胞攀附長入 ‧晶格樑柱取代實心金屬,仿骨骼結構彈性,不易沉降 ‧上下接觸表面帶有粗糙鋸齒,大幅增加摩擦力,防止術後位移 ‧多孔晶格取代實心金屬,易於X光穿透,有利術後觀察追蹤
|
1. 用於固定脊椎。 2. 脊椎椎間盤退變之脊椎前、後路手術。 3. 脊椎二次手術脊柱不穩定施行椎間盤固定手術。 4. 神經孔間狹窄。 5. 假性關節病變
|
1. 手術部位應注意避免感染。 2. 醫師應對此植入物及技術手冊有充分之研究與訓練。 3. 若病情需要,可配合其他脊椎內固定使用。 4. 醫師可依脊椎病情,當作脊椎缺損填補之用。
5. 可能影響安全及療效者包括:過度肥胖、冠心症等複雜內科疾病。
|
1. 身體對異物的過敏反應。 2. 硬脊膜破裂。 3. 因手術創傷造成神經受損、感染、延遲癒合或不癒合。 4. 植入物之抗力作用使骨密度降低。
|
1. 表面特殊處理較易增加新骨生成。 2. 具粗糙表面,增加摩擦力,防止術後內植入鬆動移位。 3.3D堆疊列印製作為立體結構更適合人體椎間盤. 4. 填補脊椎缺損增進骨融合。
|
| 寶楠耐籠頸椎三維多孔鈦合金椎間融合器 |  | 寶楠 | $95,825.00 | $19,165.00 | $76,660.00 | |
‧光滑輪廓圍繞粗糙表面,避免微創植入損傷軟組織 .頭端為拋光彈頭型設計,有利於撐開進入椎間位置,也方便術中調整植入物方向 ‧尾端具備抗衝擊結構,可承受植入過程的敲擊 ‧連通多孔結構,適合骨細胞攀附長入 ‧晶格樑柱取代實心金屬,仿骨骼結構彈性,不易沉降 ‧上下接觸表面帶有粗糙鋸齒,大幅增加摩擦力,防止術後位移 ‧多孔晶格取代實心金屬,易於X光穿透,有利術後觀察追蹤
|
治療有症狀的頸椎椎間盤退化疾病,包括頸部或手臂(神經根性)疼痛,以及經影像 檢查(電腦斷層掃描、核磁共振造影或 X 光)確認,至少出現下列任一種狀況的功能/神經 缺損:椎間盤髓核脫出突出、椎關節黏連,以及椎間盤高度縮減。
|
務必選擇合適的植入物尺寸。從包裝取出時,請先核對包裝內容物與標籤上的尺寸資 訊,檢查標籤上的印記與椎間盤高度是否符合植入物上所刻的資訊。 務必挑選適合的患者。挑選接受人工頸椎椎間盤植入的患者時,下列因素是影響手術 成功與否的關鍵:患者從事的職業或活動:是否為高齡、精神疾病、酗酒、藥物濫用患者; 是否患有特定退化性疾病,可能在植入時惡化,以致於大幅縮短裝置的預期有效壽命。 手術植入物不可重複使用或重新植入。即使裝置外觀看來並未受損,但仍可能有微小 缺陷及內部壓力問題,導致裝置提早斷裂。從最內層包裝取出帝發頸椎椎間盤及固定器時, 必須採用無菌技術。
|
裝置脫出、向後擠壓、塌陷、沈陷或位移等情形,可能造成疼痛、麻痺、血管或神經受損、脊髓受影響或損傷,或其他問題。
因裝置機械性故障或植入手術未緩解患者症狀,必須再次進行手術
脊椎不穩定, 脊椎前凸的情形發生變化, 神經狀態退化, 食道穿孔或糜爛, 脊椎面關節退化, 血拴形成, 脊椎狹窄, 椎關節黏連脊椎滑脫, 感染,早期或晚期 手術創傷或裝置造成神經受損:神經方面的問題,包括神經根性疼痛、疤痕組織,中神經糾結、肌肉無力與感覺異常。
|
1. 表面特殊處理較易增加新骨生成。 2. 具粗糙表面,增加摩擦力,防止術後內植入鬆動移位。 3.3D堆疊列印製作為立體結構更適合人體椎間盤. 4. 填補脊椎缺損增進骨融合。
|
| 寶楠耐籠三維多孔鈦合金椎間融合器(PLIF小顆) |  | 寶楠 | $114,077.00 | $22,815.00 | $91,262.00 | |
‧光滑輪廓圍繞粗糙表面,避免微創植入損傷軟組織 .頭端為拋光彈頭型設計,有利於撐開進入椎間位置,也方便術中調整植入物方向 ‧尾端具備抗衝擊結構,可承受植入過程的敲擊 ‧連通多孔結構,適合骨細胞攀附長入 ‧晶格樑柱取代實心金屬,仿骨骼結構彈性,不易沉降 ‧上下接觸表面帶有粗糙鋸齒,大幅增加摩擦力,防止術後位移 ‧多孔晶格取代實心金屬,易於X光穿透,有利術後觀察追蹤
|
1. 用於固定脊椎。 2. 脊椎椎間盤退變之脊椎前、後路手術。 3. 脊椎二次手術脊柱不穩定施行椎間盤固定手術。 4. 神經孔間狹窄。 5. 假性關節病變
|
1. 手術部位應注意避免感染。 2. 醫師應對此植入物及技術手冊有充分之研究與訓練。 3. 若病情需要,可配合其他脊椎內固定使用。 4. 醫師可依脊椎病情,當作脊椎缺損填補之用。
5. 可能影響安全及療效者包括:過度肥胖、冠心症等複雜內科疾病。
|
1. 身體對異物的過敏反應。 2. 硬脊膜破裂。 3. 因手術創傷造成神經受損、感染、延遲癒合或不癒合。 4. 植入物之抗力作用使骨密度降低。
|
1. 表面特殊處理較易增加新骨生成。 2. 具粗糙表面,增加摩擦力,防止術後內植入鬆動移位。 3.3D堆疊列印製作為立體結構更適合人體椎間盤. 4. 填補脊椎缺損增進骨融合。
|